Илоперидон (фанапт) Пълна информация за предписване
Марка: Fanapt
Родово име: Илоперидон
Ръководство за предписване на Fanapt (Iloperidone) (PDF)
Съдържание:
Боксово предупреждение
Показания и употреба
Дозировка и приложение
Противопоказания
Предупреждения и предпазни мерки
Нежелани реакции
Взаимодействия с лекарства
Използване в специфични популации
Злоупотреба с наркотици и зависимост
свръх доза
описание
Клинична фармакология
Неклинична токсикология
Клинични изследвания
Как се доставя
Ръководство за лекарства Brintellix
ПРЕДУПРЕЖДЕНИЕ: УВЕЛИЧЕНА МОРТАЛНОСТ ПРИ ПЪРВИ ПАЦИЕНТИ С ПСИХОЗА, СВЪРЗАНА С ДЕМЕНТИЯТА
Пациентите в напреднала възраст с психоза, свързани с деменция, лекувани с антипсихотични лекарства, са изложени на повишен риск от смърт. FANAPT не е одобрен за лечение на пациенти с психоза, свързана с деменция.
Показания и употреба
FANAPT® е показан за лечение на шизофрения при възрастни.
Когато решава сред алтернативните методи за лечение на това състояние, лекуващият трябва да вземе предвид констатацията, че FANAPT е свързан с удължаване на QTc интервала. Удължаването на QTc интервала е свързано с някои други лекарства със способността да причиняват torsade de аритмия тип pointes, потенциално фатална полиморфна камерна тахикардия, която може да доведе до внезапна смърт. В много случаи това би довело до заключението, че първо трябва да се опитат други лекарства. Дали FANAPT ще предизвика torsade de pointes или ще увеличи скоростта на внезапна смърт, все още не е известно.
Пациентите трябва да бъдат титрирани до ефективна доза FANAPT. По този начин контролът на симптомите може да се забави през първите 1 до 2 седмици на лечение в сравнение с някои други антипсихотични лекарства, които не изискват подобно титруване. Предписващите лекари трябва да имат предвид това забавяне, когато избират антипсихотично лекарство за лечение на шизофрения.
продължете историята по-долу
Дозировка и приложение
Обичайна доза
FANAPT трябва да се титрува бавно от ниска начална доза, за да се избегне ортостатична хипотония поради неговите алфа-адренергични блокиращи свойства. Препоръчителната начална доза за FANAPT таблетки е 1 mg перорално два пъти дневно. Увеличаването на дозата за достигане на целевия диапазон от 6 -12 mg два пъти дневно (12_24 mg / ден) може да се извършва с корекции на дневната доза, която да не надвишава 2 mg два пъти дневно (4 mg / ден). Максималната препоръчителна доза е 12 mg два пъти дневно (24 mg / ден). Дозите на FANAPT над 24 mg / ден не са систематично оценявани в клиничните проучвания. Ефикасността е доказана с FANAPT в дозов диапазон от 6 до 12 mg два пъти дневно. Предписващите лекари трябва да имат предвид факта, че пациентите трябва да бъдат титрирани до ефективна доза FANAPT. По този начин контролът на симптомите може да се забави през първите 1 до 2 седмици на лечение в сравнение с някои други антипсихотични лекарства, които не изискват подобно титруване. Предписващите лекар също трябва да са наясно, че някои нежелани ефекти, свързани с употребата на FANAPT, са свързани с дозата. FANAPT може да се прилага независимо от храненето.
Дозировка при специални популации
Коригиране на дозата за пациенти, приемащи FANAPT едновременно с потенциални инхибитори на CYP2D6: Дозата FANAPT трябва да бъде се намалява с половината, когато се прилага едновременно със силни CYP2D6 инхибитори, като флуоксетин или пароксетин. Когато инхибиторът на CYP2D6 се оттегли от комбинираната терапия, дозата FANAPT трябва да се увеличи до мястото, където е било преди.
Корекция на дозата за пациенти, приемащи FANAPT едновременно с потенциални инхибитори на CYP3A4: Дозата FANAPT трябва да бъде се намалява с половината, когато се прилага едновременно със силни CYP3A4 инхибитори като кетоконазол или кларитромицин. Когато CYP3A4 инхибиторът се оттегли от комбинираната терапия, дозата FANAPT трябва да се увеличи до мястото, където е било преди.
Корекция на дозата за пациенти, приемащи FANAPT, които са бедни метаболизатори на CYP2D6: Дозата FANAPT трябва да бъде намалена с половината при лоши метаболизатори на CYP2D6.
Чернодробно увреждане: Не е необходимо коригиране на дозата на FANAPT при пациенти с леко чернодробно увреждане. Пациентите с умерено чернодробно увреждане може да изискват намаляване на дозата, ако е клинично показано. FANAPT не се препоръчва на пациенти с тежко чернодробно увреждане.
Поддържащо лечение
В по-дългосрочно проучване FANAPT е ефективен за забавяне на времето за рецидив при пациенти с шизофрения, които са били стабилизирани на FANAPT до 24 mg / ден. Периодично трябва да се преценяват пациентите, за да се определи необходимостта от поддържащо лечение.
Повторно прекратяване на лечението при пациенти, прекъснато по-рано Въпреки че няма данни, които да се занимават конкретно с повторното лечение лечение, се препоръчва схемата за начало на титруване да се спазва всеки път, когато пациентите са имали интервал извън FANAPT от повече повече от 3 дни.
Горна част
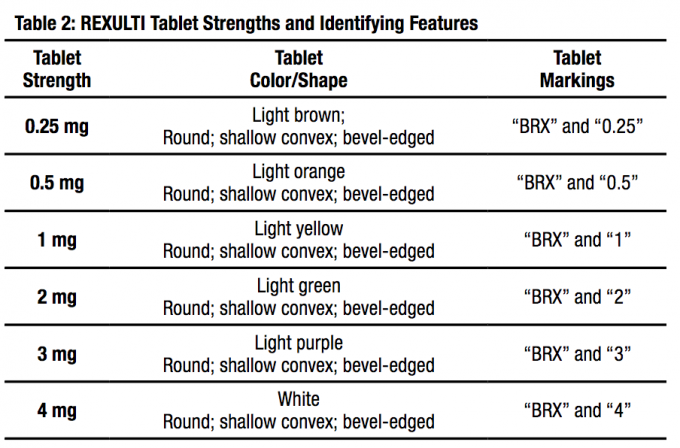
Лекарствени форми и силни страни
FANAPT таблетки се предлагат в следните силни стойности: 1 mg, 2 mg, 4 mg, 6 mg, 8 mg, 10 mg и 12 mg. Таблетките са бели, кръгли, плоски, със скосени ръбове и се идентифицират с лого „”, вдлъбнато от едната страна и сила на таблета „1”, „2”, „4”, „6”, „8”, „10”, или „12”, релефно от другата страна.
Горна част
Противопоказания
FANAPT е противопоказан при хора с известна реакция на свръхчувствителност към продукта. Съобщава се за анафилаксия, ангиоедем и други реакции на свръхчувствителност.
Горна част
ПРЕДУПРЕЖДЕНИЯ И МЕРКИ ЗА ПРЕДУПРЕЖДЕНИЕ
Повишена смъртност при пациенти в напреднала възраст с психоза, свързана с деменция
Антипсихотичните лекарства увеличават всички причини за смърт при пациенти в напреднала възраст с психоза, свързана с деменция. Анализи на 17 свързани с деменция психоза плацебо-контролирани проучвания (модална продължителност 10 седмици и до голяма степен при пациенти, приемащи атипични антипсихотични лекарства) разкрива риск от смърт при лекуваните с наркотици пациенти между 1,6 до 1,7 пъти по-висок от този при пациенти, лекувани с плацебо. В хода на типично 10-седмично контролирано проучване, процентът на смърт при пациенти, лекувани с наркотици, е около 4,5%, в сравнение със скорост от около 2,6% при пациенти, лекувани с плацебо.
Въпреки че причините за смъртта са разнообразни, повечето от смъртните случаи изглежда са били сърдечно-съдови (например сърдечна недостатъчност, внезапна смърт) или инфекциозни (например пневмония). FANAPT не е одобрен за лечение на пациенти с психоза, свързана с деменция.
Цереброваскуларни нежелани реакции, включително инсулт, при пациенти в напреднала възраст с психоза, свързана с деменция
В плацебо-контролирани проучвания при пациенти в напреднала възраст с деменция, пациенти, рандомизирани на рисперидон, арипипразол и оланзапин имат по-висока честота на инсулт и преходна исхемична атака, включително фатална удар. FANAPT не е одобрен за лечение на пациенти с психоза, свързана с деменция.
Удължаване на QT
В открито проучване на QTc при пациенти с шизофрения или шизоафективно разстройство (n = 160), FANAPT се свързва с удължаване на QTc с 9 msec при доза илоперидон 12 mg два пъти дневно. Ефектът на FANAPT върху QT интервала се усилва от наличието на метаболитно инхибиране на CYP450 2D6 или 3A4 (пароксетин 20 mg веднъж дневно и кетоконазол 200 mg два пъти дневно, съответно). При условия на метаболитно инхибиране както за 2D6, така и за 3А4, FANAPT 12 mg два пъти дневно се свързва със средно увеличение на QTcF от изходната стойност от около 19 msec.
Не са наблюдавани случаи на torsade de pointes или други тежки сърдечни аритмии по време на клиничната програма преди пускане на пазара.
Употребата на FANAPT трябва да се избягва в комбинация с други лекарства, за които е известно, че удължават QTc, включително клас 1А (например хинидин, прокаинамид) или клас III (например, амиодарон, соталол) антиаритмични лекарства, антипсихотични лекарства (например хлорпромазин, тиоридазин), антибиотици (например, гатифлоксацин, моксифлоксацин) или всеки друг клас лекарства, за които е известно, че удължават QTc интервала (например, пентамидин, левометадилацетат, метадон). FANAPT също трябва да се избягва при пациенти с вроден дълъг QT синдром и при пациенти с анамнеза за сърдечна аритмия.
Определени обстоятелства могат да увеличат риска от torsade de pointes и / или внезапна смърт във връзка с употребата на лекарства, които удължават QTc интервала, включително (1) брадикардия; (2) хипокалиемия или хипомагнезиемия; (3) едновременна употреба на други лекарства, които удължават интервала QTc; и (4) наличие на вродено удължаване на QT интервала; (5) скорошен остър миокарден инфаркт; и / или (6) некомпенсирана сърдечна недостатъчност.
Необходимо е внимание, когато се предписва FANAPT с лекарства, които инхибират метаболизма на FANAPT, и при пациенти с намалена активност на CYP2D6.
Препоръчва се пациентите да бъдат разглеждани за лечение с FANAPT, които са изложени на значителен риск електролитни нарушения имат изходни измервания на серумния калий и магнезий с периодични мониторинг. Хипокалемията (и / или хипомагнезиемия) може да увеличи риска от удължаване на QT и аритмия. FANAPT трябва да се избягва при пациенти със значими сърдечно-съдови заболявания, например QT удължаване, скорошен остър миокарден инфаркт, некомпенсирана сърдечна недостатъчност или сърдечна аритмия. FANAPT трябва да се прекрати при пациенти, за които е установено, че имат постоянни QTc измервания> 500 msec.
Ако пациентите, приемащи FANAPT, изпитват симптоми, които биха могли да показват появата на сърдечни аритмии, напр. замаяност, сърцебиене или синкоп, предписващият лекар трябва да започне допълнителна оценка, включително сърдечна мониторинг.
Невролептичен злокачествен синдром (NMS)
Съобщава се за потенциално фатален симптомен комплекс, понякога наричан невролептичен злокачествен синдром (НМС) във връзка с прилагането на антипсихотични лекарства, включително FANAPT. Клиничните прояви включват хиперпирексия, мускулна ригидност, променен умствен статус (включително кататонични признаци) и доказателства за автономна нестабилност (неравномерен пулс или кръвно налягане, тахикардия, диафореза и сърдечно аритмия). Допълнителни признаци могат да включват повишена креатинфосфокиназа, миоглобинурия (рабдомиолиза) и остра бъбречна недостатъчност. Диагностичната оценка на пациенти с този синдром е сложна. При постигането на диагноза е важно да се идентифицират случаите, в които клиничното представяне включва както сериозно медицинско заболяване, така и нелекувани или неадекватно лекувани екстрапирамидни признаци и симптоми (EPS). Други важни съображения в диференциалната диагноза включват централна антихолинергична токсичност, топлинен удар, лекарствена треска и патология на централната нервна система (ЦНС).
Управлението на този синдром трябва да включва: (1) незабавно прекратяване на антипсихотичните лекарства и други лекарства, които не са от съществено значение за едновременната терапия, (2) интензивно симптоматично лечение и медицински мониторинг и (3) лечение на всички съпътстващи сериозни медицински проблеми, за които се предлагат специфични лечения. Няма общо съгласие за специфични схеми на фармакологично лечение на НМС.
Ако пациентът се нуждае от лечение с антипсихотични лекарства след възстановяване от НМС, трябва да се обмисли внимателно потенциалното повторно въвеждане на лекарствена терапия. Пациентът трябва да бъде внимателно наблюдаван, тъй като са съобщени рецидиви на НМС.
Тардивна дискинезия
Тардивна дискинезия е синдром, състоящ се от потенциално необратими, неволни, дискинетични движения, които могат да се развият при пациенти, лекувани с антипсихотични лекарства. Въпреки че разпространението на синдрома изглежда най-високо сред възрастните хора, особено възрастните жени, това е невъзможно разчитат на прогнозите за разпространение, за да прогнозират при започване на антипсихотично лечение, което пациентите вероятно ще развият синдром. Дали антипсихотичните лекарствени продукти се различават по своя потенциал да причинят тардивна дискинезия.
Вярва се рискът от развитие на тардивна дискинезия и вероятността тя да стане необратима да се увеличи с продължителността на лечението и общата кумулативна доза на прилаганите антипсихотици се увеличава. Синдромът обаче може да се развие, макар и много по-рядко, след сравнително кратки периоди на лечение при ниски дози.
Не е известно лечение за установени случаи на тардивна дискинезия, въпреки че синдромът може да отстъпи, частично или напълно, ако антипсихотичното лечение бъде отменено. Самото антипсихотично лечение обаче може да потисне (или частично да потисне) признаците и симптомите на синдрома и по този начин евентуално да маскира основния процес. Ефектът, който симптоматичното потискане има върху дългосрочния ход на синдрома, е неизвестен.
Като се имат предвид тези съображения, FANAPT трябва да се предписва по начин, който е най-вероятно да сведе до минимум появата на тардивна дискинезия. Хроничното антипсихотично лечение обикновено трябва да бъде запазено за пациенти, които страдат от хронично заболяване, на което (1) е известно, че реагира антипсихотични лекарства и (2), за които не са налични алтернативни, еднакво ефективни, но потенциално по-малко вредни лечения или уместно. При пациенти, които се нуждаят от хронично лечение, трябва да се търси най-малката доза и най-кратката продължителност на лечението, което води до задоволителен клиничен отговор. Необходимостта от продължително лечение трябва периодично да се преоценява.
Ако признаци и симптоми на тардивна дискинезия се появят при пациент на FANAPT, трябва да се обмисли прекратяване на лекарството. Въпреки това, някои пациенти могат да изискват лечение с FANAPT, въпреки наличието на синдрома.
Метаболитни промени
Атипичните антипсихотични лекарства са свързани с метаболитни промени, които могат да повишат сърдечно-съдовия / мозъчно-съдовия риск. Тези метаболитни промени включват хипергликемия, дислипидемия и наддаване на телесно тегло. Въпреки че е показано, че всички нетипични антипсихотични лекарства произвеждат някои метаболитни промени, всяко лекарство в класа има свой специфичен рисков профил.
Хипергликемия и захарен диабет
Съобщава се за хипергликемия, в някои случаи екстремна и свързана с кетоацидоза или хиперосмоларна кома или смърт, при пациенти, лекувани с нетипични антипсихотици, включително FANAPT. Оценката на връзката между нетипичната антипсихотична употреба и отклоненията в глюкозата се усложнява от възможността за увеличаване основен риск от захарен диабет при пациенти с шизофрения и нарастващата честота на захарния диабет като цяло население. Като се имат предвид тези обърквачи, връзката между нетипичната антипсихотична употреба и нежеланите събития, свързани с хипергликемия, не е напълно разбрана. Въпреки това епидемиологичните проучвания предполагат повишен риск от нежелани събития, свързани с хипергликемия при пациенти, лекувани с атипичните антипсихотици, включени в тези проучвания.
Пациентите с установена диагноза захарен диабет, които са започнати с атипични антипсихотици, трябва редовно да се наблюдават за влошаване на контрола на глюкозата. Пациенти с рискови фактори за захарен диабет (напр. Затлъстяване, фамилна анамнеза за диабет), които започват лечение с атипичните антипсихотици трябва да се подлагат на изследване на кръвната захар на гладно в началото на лечението и периодично по време на лечение. Всеки пациент, лекуван с атипични антипсихотици, трябва да бъде наблюдаван за симптоми на хипергликемия, включително полидипсия, полиурия, полифагия и слабост. Пациентите, които развиват симптоми на хипергликемия по време на лечение с нетипични антипсихотици, трябва да се подлагат на тест за кръвна захар на гладно. В някои случаи хипергликемията отшумява при прекратяване на нетипичния антипсихотик; въпреки това, някои пациенти се нуждаят от продължаване на антидиабетно лечение, въпреки прекратяването на подозрителното лекарство.
Данни от проучване с фиксирана доза при възрастни лица с шизофрения, в което са взети кръвни проби на гладно, са представени в таблица 1.
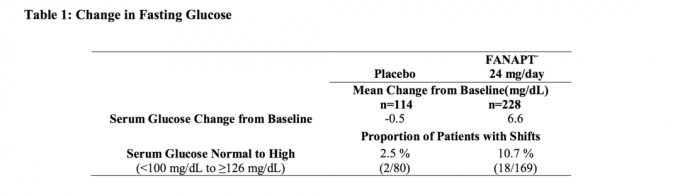
Сборни анализи на данни за глюкоза от клинични проучвания, включително по-продължителни изпитвания, са показани в таблица2.
дислипидемия
Нежелани промени в липидите са наблюдавани при пациенти, лекувани с нетипични антипсихотици.
Данни от контролирано плацебо, 4-седмично проучване с фиксирана доза, в което са взети кръвни проби на гладно, при възрастни лица с шизофрения са представени в таблица 3.

Сборните анализи на данни за холестерола и триглицеридите от клинични проучвания, включително по-дългосрочни изпитвания, са показани в таблица 4 и таблица 5.
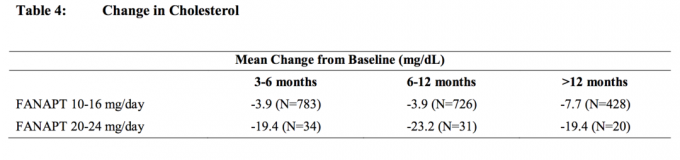
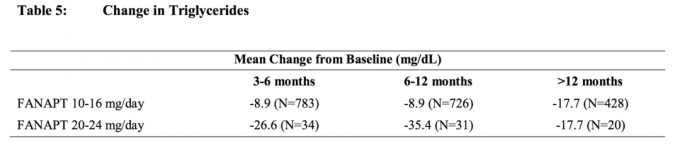
Качване на тегло
Наблюдава се наддаване на тегло при нетипична антипсихотична употреба. Препоръчва се клинично наблюдение на теглото.
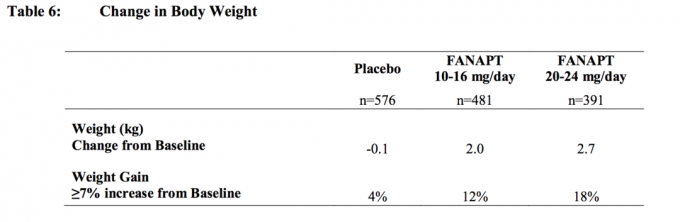
В рамките на всички краткосрочни и дългосрочни проучвания общата средна промяна от базовата стойност в крайната точка е 2,1 kg.
Промени в телесното тегло (kg) и съотношението на пациентите с ≥7% наддаване в телесното тегло от 4 са представени плацебо-контролирани, 4- или 6-седмични, фиксирани или гъвкави дози при възрастни лица Таблица 6.
Припадъци
В краткосрочни плацебо-контролирани проучвания (4- до 6-седмици) припадъци са се появили при 0,1% (1/1344) от пациентите, лекувани с FANAPT, в сравнение с 0,3% (2/587) на плацебо. Както при другите антипсихотици, FANAPT трябва да се използва предпазливо при пациенти с анамнеза за гърчове или със състояния, които потенциално понижават прага на пристъпите. Условията, които понижават прага на припадък, могат да бъдат по-разпространени при популация от 65 години или повече.
Ортостатична хипотония и синкоп
FANAPT може да предизвика ортостатична хипотония, свързана със световъртеж, тахикардия и синкоп. Това отразява неговите алфа1-адренергични антагонистични свойства. При двойно слепи плацебо-контролирани краткосрочни проучвания, при които дозата се повишава бавно, както се препоръчва по-горе, синкоп е отчетен при 0,4% (5/1344) от пациентите, лекувани с FANAPT, в сравнение с 0,2% (1/587) на плацебо. Има съобщения за ортостатична хипотония при 5% от пациентите, получаващи 20-24 mg / ден, 3% от пациентите, които са получавали 10-16 mg / ден, и 1% от пациентите, получавали плацебо. Очаква се по-бързото титруване да увеличи скоростта на ортостатична хипотония и синкоп.
FANAPT трябва да се използва с повишено внимание при пациенти с известни сърдечно-съдови заболявания (например сърдечна недостатъчност, анамнеза за миокарден инфаркт, исхемия или проводимост аномалии), мозъчносъдова болест или състояния, които предразполагат пациента към хипотония (дехидратация, хиповолемия и лечение с антихипертензивна лекарства). Трябва да се има предвид наблюдението на ортостатичните жизнени показатели при пациенти, които са уязвими към хипотония.
Левкопения, неутропения и агранулоцитоза
В клинични изпитвания и постмаркетингов опит се съобщава за събития на левкопения / неутропения, свързани временно с антипсихотични средства. Съобщава се и за агранулоцитоза (включително фатални случаи).
Възможните рискови фактори за левкопения / неутропения включват съществуващ нисък брой на белите кръвни клетки (WBC) и анамнеза за индуцирана от лекарства левкопения / неутропения. Пациентите с предшестваща ниска WBC или анамнеза за индуцирана от лекарства левкопения / неутропения трябва да имат пълен контрол на кръвната картина (CBC) често през първите няколко месеца на терапия и трябва да прекъсне FANAPT при първите признаци на спад на WBC при липса на друга причинител фактори.
Пациентите с неутропения трябва внимателно да се наблюдават за треска или други симптоми или признаци на инфекция и да се лекуват незабавно, ако се появят такива симптоми или признаци. Пациентите с тежка неутропения (абсолютен брой неутрофили <1000 / mm3) трябва да преустановят FANAPT и да следят техния WBC до възстановяване.
хиперпролактинемия
Както при другите лекарства, които антагонизират рецепторите на допамин D2, FANAPT повишава нивата на пролактин.
Хиперпролактинемията може да потисне хипоталамичния GnRH, което води до намалена секреция на гонадотропин на хипофизата. Това от своя страна може да попречи на репродуктивната функция, като наруши гонадалстероидогенезата както при жени, така и при мъже. Съобщава се за галакторея, аменорея, гинекомастия и импотентност с пролактин-повишаващи съединения. Дълготрайната хиперпролактинемия, свързана с хипогонадизъм, може да доведе до намаляване на костната плътност както при жените, така и при мъжете.
Експериментите с тъканна култура показват, че приблизително една трета от човешки рак на гърдата са пролактинозависими in vitro, a фактор от потенциално значение, ако се предвижда предписване на тези лекарства при пациент с предварително открита гърда рак. Пролиферативни промени и повишаване на серумния пролактин на млечната жлеза са наблюдавани при мишки и плъхове, лекувани с FANAPT. Нито клиничните проучвания, нито епидемиологичните проучвания, проведени до момента, не показват връзка между хроничното приложение на този клас лекарства и туморогенезата при хора; наличните доказателства се считат за твърде ограничени, за да бъдат окончателни в момента.
В краткосрочно плацебо-контролирано проучване (4 седмици) средната промяна от началната до крайната точка в плазмените нива на пролактин за групата, третирана с FANAPT 24 mg / ден, е увеличение с 2,6 ng / mL в сравнение с понижение от 6,3 ng / mL в плацебо група. В това проучване са наблюдавани повишени плазмени нива на пролактин при 26% от възрастните, лекувани с FANAPT, в сравнение с 12% в групата на плацебо. В краткосрочните изпитвания FANAPT се свързва със скромни нива на повишаване на пролактина в сравнение с по-големите повишения на пролактина, наблюдавани при някои други антипсихотични средства. При обединен анализ от клинични проучвания, включващи по-продължителни изпитвания, при 3210 възрастни, лекувани с илоперидон, е съобщено за гинекомастия при 2 мъже (0,1%) в сравнение с 0% при пациенти, лекувани с плацебо, и галакторея се съобщава при 8 жени (0,2%) в сравнение с 3 жени (0,5%) при лекувани с плацебо пациенти.
Регулация на телесната температура
Нарушаването на способността на организма да понижава телесната телесна температура се дължи на антипсихотичните средства. Препоръчва се подходяща грижа при предписване на FANAPT за пациенти, при които се наблюдават състояния, които могат да допринесат за повишаване на телесното тяло температура, напр. упражняване усилено, излагане на силна топлина, прием на съпътстващи лекарства с антихолинергична активност или подлагане на обезводняване.
Дисфагия
Дисофилността и аспирацията на хранопровода са свързани с употребата на антипсихотични лекарства. Аспирационната пневмония е честа причина за заболеваемост и смъртност при пациенти в напреднала възраст. FANAPT и други антипсихотични лекарства трябва да се използват предпазливо при пациенти с риск от аспирационна пневмония.
самоубийство
Възможността за опит за самоубийство е присъща на психотични заболявания и внимателното наблюдение на високорисковите пациенти трябва да придружава лекарствената терапия. Предписанията за FANAPT трябва да бъдат написани за най-малкото количество таблетки, съобразено с доброто управление на пациента, за да се намали рискът от предозиране.
приапизъм
Три случая на приапизъм са докладвани в програмата за пускане на пазара FANAPT. Съобщава се, че лекарства с алфа-адренергични блокиращи ефекти предизвикват приапизъм. FANAPT споделя тази фармакологична активност. Тежкият приапизъм може да изисква хирургическа намеса.
Потенциал за когнитивно и двигателно увреждане
FANAPT, подобно на други антипсихотици, има потенциал да влоши преценката, мисленето или двигателните умения. В краткосрочни, плацебо-контролирани проучвания, сънолентност (включително седатиране) е отчетена при 11,9% (104/874) от възрастни пациенти, лекувани с FANAPT в дози от 10 mg / ден или повече срещу 5.3% (31/587), лекувани с плацебо. Пациентите трябва да бъдат предупредени относно експлоатацията на опасни машини, включително автомобили, докато не са сигурни, че терапията с FANAPT не им влияе неблагоприятно.
Горна част
Нежелани реакции
Опит с клинични изследвания
Тъй като клиничните изпитвания се провеждат при много различни условия, честотата на нежеланите реакции се наблюдава при клиничното изпитване на лекарство не може да бъде пряко сравняван с процентите в клиничните изпитвания на друго лекарство и може да не отразява честотата, наблюдавана в клиничните практикуват. Информацията по-долу е получена от база данни за клинични изпитвания за FANAPT, състояща се от 3229 пациенти, изложени на FANAPT в дози от 10 mg / ден или повече, за лечение на шизофрения. От тях 999 са получили FANAPT за най-малко 6 месеца, като 657 са били изложени на FANAPT за най-малко 12 месеца. Всички тези пациенти, които са получавали FANAPT, са участвали в клинични изпитвания с много дози. Условията и продължителността на лечението с FANAPT варира значително и включва (в категориите за припокриване), отворени етикети и двойно слепи фази на проучвания, стационарни и амбулаторни, фиксирани дози и гъвкави дози, както и краткосрочни и дългосрочни експозиция.
Информацията, представена в тези раздели, е получена от обединени данни от 4 плацебо контролирани, 4- или 6-седмични, изследвания с фиксирана или гъвкава доза при пациенти, които са получавали FANAPT в дневни дози в диапазон от 10 до 24 mg (П = 874).
Нежелани реакции, възникващи при честота от 2% или повече сред пациентите, лекувани с FANAPT и по-често срещани от плацебо
Таблица 7 изброява групираните случаи на нежелани реакции, за които спонтанно се съобщава при четири плацебо-контролирани, 4- или 6-седмични, изследвания с фиксирана или гъвкава доза, в които са изброени онези реакции, възникнали при 2% или повече пациенти, лекувани с FANAPT във всяка от дозите групи и за които честотата при лекувани с FANAPT пациенти във всяка група на дозата е била по-голяма от честотата при пациенти, лекувани с плацебо.
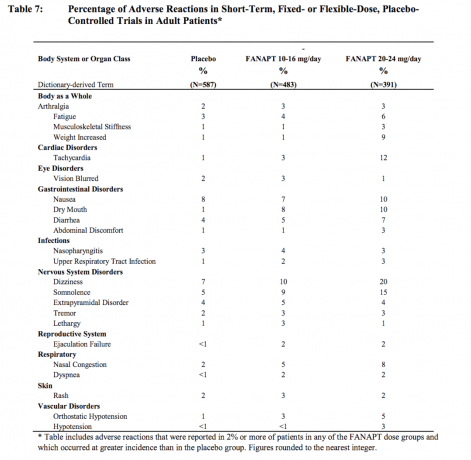
Нежелани реакции, свързани с дозата при клинични изпитвания
Въз основа на събраните данни от 4 плацебо-контролирани, 4- или 6-седмични проучвания с фиксирана или гъвкава доза, нежелани реакции, възникнали с повече от 2% честота при пациенти, лекувани с FANAPT, и за които честотата при пациенти, лекувани с FANAPT 20-24 mg / ден, е била два пъти по-голяма от честотата при пациенти, лекувани с FANAPT 10 -16 mg / ден, са: дискомфорт в корема, замаяност, хипотония, мускулно-скелетна скованост, тахикардия и тегло увеличен.
Чести и свързани с лекарствата нежелани реакции при клинични изпитвания
Въз основа на събраните данни от 4 плацебо-контролирани, 4- или 6-седмични проучвания с фиксирана или гъвкава доза, следните нежелани реакции са настъпили при честота ≥5% при лекуваните пациенти с FANAPT и поне два пъти плацебо плъх за поне 1 доза: замаяност, сухота в устата, умора, запушване на носа, сънливост, тахикардия, ортостатична хипотония и тегло увеличен. Замайване, тахикардия и повишаване на теглото са били поне два пъти по-чести при 20-24 mg / ден, отколкото при 10-16 mg / ден.
Екстрапирамидни симптоми (EPS) в клинични изпитвания
Събраните данни от 4-те плацебо-контролирани, 4- или 6- седмични, фиксирани или гъвкави дози предоставят информация относно EPS. Данните за нежеланите събития, събрани от тези изпитвания, показват следните нива на нежелани събития, свързани с EPS, както е показано в таблица 8.

Нежелани реакции, свързани с преустановяване на лечението при клинични изпитвания
Въз основа на събраните данни от 4 плацебо-контролирани, 4- или 6-седмични, фиксирани или гъвкави изследвания на дозата, няма разлика в честотата на прекратяване на лечението поради нежелани събития между лекуваните с FANAPT (5%) и лекуваните с плацебо (5%) пациенти. Видовете нежелани събития, които доведоха до прекратяване, бяха сходни за пациентите, лекувани с FANAPT и плацебо.
Демографски разлики в нежеланите реакции при клиничните изпитвания
Изследване на популационни подгрупи в 4-те плацебо-контролирани, 4- или 6-седмични, фиксирани или проучвания с гъвкава доза не разкриха никакви доказателства за разлики в безопасността на базата на възрастта, пол или раса.
Отклонения в лабораторните изследвания в клиничните изпитвания
Няма разлики между FANAPT и плацебо в честотата на прекъсване поради промени в хематологията, анализа на урината или серумната химия.
В краткосрочните плацебо-контролирани проучвания (4-6 седмици) е имало 1,0% (13/1342) пациенти, лекувани с илоперидон с хематокрит поне един път под разширения нормален диапазон по време на лечението след рандомизация, в сравнение с 0,3% (2/585) на плацебо. Разширеният нормален диапазон за понижен хематокрит беше определен във всяко от тези изпитвания като стойността с 15% под нормалния диапазон за централизираната лаборатория, която беше използвана в изпитването.
Други реакции по време на предварителната маркетингова оценка на FANAPT
Следва списък на термините MedDRA, които отразяват нежеланите реакции при пациенти, лекувани с FANAPT при многократни дози ≥ 4 mg / ден по време на всяка фаза на изпитване с базата данни от 3210, лекувани с FANAPT пациенти. Всички докладвани реакции са включени, с изключение на вече изброените в таблица 7, или други части от нежеланите реакции (6), тези, разгледани в Предупреждения и предпазни мерки (5), термините на реакция, които са толкова общи, че са неинформативни, съобщени реакции при по-малко от 3 пациенти и които не са нито сериозни, нито животозастрашаващи, реакции, които иначе са често срещани като фонови реакции, и реакции, считани за малко вероятно да бъдат лекарства свързани.
Реакциите се категоризират допълнително от системния орган на MedDRA и са изброени в ред на намаляваща честота, както следва дефиниции: честите нежелани реакции са тези, които се срещат при най-малко 1/100 пациенти (само тези, които не са изброени в таблица 7, се появяват в това листинг); редки нежелани реакции са тези, които се проявяват при 1/100 до 1/1000 пациенти; редки събития са тези, които се срещат при по-малко от 1/1000 пациенти.
Кръвни и лимфни нарушения: Често - анемия, желязодефицитна анемия; Редки-левкопения
Сърдечни нарушения: Чести - сърцебиене; Редки - аритмия, атриовентрикуларен блок първа степен, сърдечна недостатъчност (включително застойна и остра)
Ушни и лабиринтни нарушения: рядко - световъртеж, шум в ушите
Ендокринни нарушения: Често - хипотиреоидизъм
Очни нарушения: Чести - конюнктивит (включително алергичен); Често - сухо око, блефарит, оток на клепачите, оток на очите, непрозрачност на лещата, катаракта, хиперемия (включително конюнктивална)
Стомашно-чревни разстройства: рядко - гастрит, слюнчена хиперсекреция, фекална инконтиненция, улцерация на устата; Редки - афтозен стоматит, язва на дванадесетопръстника, хиатусна херния, хиперхлорхидрия, язва на устните, рефлуксен езофагит, стоматит
Общи нарушения и административни условия на място: рядко - оток (общ, язви, поради сърдечно заболяване), затруднено ходене, жажда; Редки - хипертермия
Хепатобилиарни нарушения: Често - холелитиаза
Изследвания: Често: тегло намалява; Често - хемоглобинът намалява, броят на неутрофилите се увеличава, хематокритът намалява
Метаболизъм и хранителни разстройства: рядко - повишен апетит, дехидратация, хипокалиемия, задържане на течности
Мускулно-скелетни и съединителни тъканни нарушения: Чести - миалгия, мускулни спазми; Редки - тортиколис
Нарушения на нервната система: Често-парестезия, психомоторна хиперактивност, безпокойство, амнезия, нистагъм; Редки - синдром на неспокойните крака
Психични разстройства: Често - неспокойствие, агресия, заблуда; Редки - враждебност, либидо намалено, параноя, аноргазмия, конфузионно състояние, мания, кататония, промени в настроението, паника атака, обсесивно-компулсивно разстройство, булимия нерва, делириум, полидипсия психогенно, импулсно контрол, разстройство депресия
Бъбречни и пикочни нарушения: Често - уринарна инконтиненция; Редки - дизурия, полакиурия, енуреза, нефролитиаза; Редки - задържане на урина, остра бъбречна недостатъчност
Репродуктивна система и нарушения на гърдата: Често - еректилна дисфункция; Infrequen - болка в тестисите, аменорея, болка в гърдите; Редки - менструация нередовна, гинекомастия, менорагия, метрорагия, постменопаузален кръвоизлив, простатит.
Респираторни, гръдни и медиастинални нарушения: Често - епистаксис, астма, ринорея, задръстване на синусите, сухота в носа; Редки - сухота в гърлото, синдром на сънна апнея, задух
Опит след постмаркетинг
По време на употребата на FANAPT са установени следните нежелани реакции: ретроградна еякулация и реакции на свръхчувствителност (включително анафилаксия; ангиоедем; стягане в гърлото; орофарингеален оток; подуване на лицето, устните, устата и езика; уртикария; обрив; и сърбеж). Тъй като тези реакции са съобщени доброволно от популация с несигурен размер, не е възможно надеждно да се прецени тяхната честота или да се установи причинно-следствена връзка с експозицията на лекарства.
Горна част
Взаимодействия с лекарства
Като се имат предвид основните ефекти върху FANAPT върху ЦНС, трябва да се внимава, когато се приема в комбинация с други централно действащи лекарства и алкохол. Благодарение на своя антагонизъм на алфа-адренергичните рецептори, FANAPT има потенциала да засили ефекта на някои антихипертензивни средства.
Потенциал за други лекарства, които да повлияят на FANAPT
Илоперидонът не е субстрат за ензимите CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19 или CYP2E1. Това предполага, че взаимодействие на илоперидон с инхибитори или индуктори на тези ензими или други фактори, като тютюнопушенето, е малко вероятно. И CYP3A4, и CYP2D6 са отговорни за метаболизма на илоперидон. Инхибиторите на CYP3A4 (например, кетоконазол) или CYP2D6 (например, флуоксетин, пароксетин) могат да инхибират елиминирането на илоперидон и да причинят повишени нива в кръвта.
Кетоконазол: Едновременно приложение на кетоконазол (200 mg два пъти дневно в продължение на 4 дни), мощен инхибитор на CYP3A4, с 3 mg еднократна доза илоперидон до 19 здрави доброволци, на възраст 18-45 години, увеличават площта под кривата (AUC) на илоперидон и неговите метаболити P88 и P95 с 57%, 55% и 35%, съответно. Дозите на илоперидон трябва да бъдат намалени с около половината, когато се прилагат с кетоконазол или други силни инхибитори на CYP3A4 (например, итраконазол). Не са проучвани по-слаби инхибитори (напр. Еритромицин, сок от грейпфрут). Когато инхибиторът на CYP3A4 се изтегли от комбинираната терапия, дозата илоперидон трябва да се върне на предишното ниво.
Флуоксетин: Съвместното приложение на флуоксетин (20 mg два пъти дневно в продължение на 21 дни), мощен инхибитор на CYP2D6, с еднократна доза от 3 mg илоперидон на 23 здрави доброволци, на възраст 29-44 години, които бяха класифицирани като обширни метаболизатори на CYP2D6, повишиха AUC на илоперидон и неговия метаболит P88, с около 2 до 3 пъти и намалиха AUC на неговия метаболит P95 с половина. Дозите на илоперидон трябва да се намалят с половината, когато се прилага с флуоксетин. Когато флуоксетин се оттегли от комбинираната терапия, дозата илоперидон трябва да се върне на предишното ниво. Очаква се други силни инхибитори на CYP2D6 да имат сходни ефекти и да се нуждаят от подходящи намаления на дозата. Когато CYP2D6 инхибиторът бъде изтеглен от комбинираната терапия, дозата на илоперидон може да бъде увеличена до предишното ниво.
Пароксетин: Съвместно приложение на пароксетин (20 mg / ден в продължение на 5-8 дни), мощен инхибитор на CYP2D6, с множество дози илоперидон (8 или 12 mg два пъти дневно) за пациенти с шизофрения на възраст 18-65 години, довело до повишени средни стационарни пикови концентрации на илоперидон и неговият метаболит P88, около 1,6 пъти, и понижават средните пикови концентрации на стационарното състояние на неговия метаболит P95 с половина. Дозите на илоперидон трябва да бъдат намалени с половината, когато се прилагат с пароксетин. Когато пароксетинът се оттегли от комбинираната терапия, дозата илоперидон трябва да се върне на предишното ниво. Очаква се други силни инхибитори на CYP2D6 да имат сходни ефекти и да се нуждаят от подходящи намаления на дозата. Когато CYP2D6 инхибиторът се оттегли от комбинираната терапия, дозата на илоперидон може да бъде увеличена до предишни нива.
Пароксетин и кетоконазол: Съвместно приложение на пароксетин (20 mg веднъж дневно в продължение на 10 дни), инхибитор на CYP2D6 и кетоконазол (200 mg два пъти дневно) с многократни дози илоперидон (8 или 12 mg два пъти дневно) при пациенти с шизофрения на възраст 18-65 години води до 1.4 увеличение на кратността на стационарните концентрации на илоперидон и неговия метаболит Р88 и 1,4-кратно намаляване на Р95 в присъствието на пароксетин. Така че даването на илоперидон с инхибитори на двата му метаболитни пътя не доведе до ефекта на нито един от инхибиторите, дадени самостоятелно. Следователно дозите на илоперидон трябва да бъдат намалени с около половината, ако се прилагат едновременно и с инхибитор на CYP2D6, и на CYP3A4.
Потенциал за FANAPT да повлияе на други лекарства
Проучванията in vitro при микрозоми на черния дроб при хора показват, че илоперидонът не инхибира съществено метаболизма на лекарства, метаболизирани от следните изоцими на цитохром Р450: CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9 или CYP2E1. Освен това, in vitro проучвания при човешки чернодробни микрозоми показват, че илоперидонът няма ензимна индукция свойства, специално за следните цитохром Р450 изозими: CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP3A4 и CYP3A5.
Декстрометорфан: Изследване при здрави доброволци показа, че промените във фармакокинетиката на декстрометорфан (доза от 80 mg), когато 3 mg доза от илоперидонът се прилага едновременно, което води до 17% увеличение на общата експозиция и 26% увеличение на максималните плазмени концентрации C max на декстрометорфан. По този начин взаимодействие между илоперидон и други субстрати на CYP2D6 е малко вероятно.
Флуоксетин: Еднократна доза от 3 mg илоперидон не оказва влияние върху фармакокинетиката на флуоксетин (20 mg два пъти дневно).
Мидазолам (чувствителен субстрат на CYP 3A4): Изследване при пациенти с шизофрения показва по-малко от 50% увеличение на мидазолам експозиция в стабилно състояние на илоперидон (14 дни перорално приложение до 10 mg илоперидон два пъти дневно) и няма ефект върху мидазолам С макс. По този начин взаимодействие между илоперидон и други субстрати на CYP3A4 е малко вероятно.
Лекарства, които удължават QT Interval FANAPT, не трябва да се използват с други лекарства, които удължават QT интервала.
Горна част
Използвайте в конкретни популации
Регистър на експозицията на бременност
Съществува регистър на експозиция на бременност, който следи резултатите от бременността при жени, изложени на FANAPT по време на бременност. За повече информация се свържете с Националния регистър за бременност за атипични антипсихотици на 1-866-961-2388 или посетете http://womensmentalhealth.org/clinical-and -research-програми / pregnancyregistry /.
Обобщение на риска
Новородени, чиито майки са изложени на антипсихотични лекарства, включително FANAPT, през третия триместър на бременността са изложени на риск от екстрапирамидни и / или симптоми на отнемане след раждането. Ограничените налични данни с FANAPT при бременни жени не са достатъчни, за да информират риска, свързан с наркотици за големи вродени дефекти и спонтанен аборт. Илоперидонът не е тератогенен, когато се прилага перорално на бременни плъхове по време на органогенеза в дози до 26 пъти над максималната препоръчителна доза от 24 mg / ден на база mg / m2. Въпреки това, той удължава продължителността на бременността и раждането, увеличава още ражданията, ранната вътрематочна смърт, увеличава честотата на забавяне на развитието и намалява преживяемостта на раждането след раждане. Илоперидонът не е тератогенен, когато се прилага перорално на бременни зайци по време на органогенеза в дози до 20 пъти по-малко от MRHD на mg / m2 основа. Въпреки това, тя увеличи ранната вътрематочна смърт и намали жизнеспособността на плода при най-високата доза, която също беше токсична за майката доза.
Основният риск от големи дефекти при раждане и спонтанен аборт за посочената популация не е известен. В американската обща популация приблизителният риск от основни вродени дефекти и спонтанен аборт при клинично признати бременности е съответно 2-4% и 15-20%.
Клинични съображения
Нежелани реакции на плода / новороденото
Екстрапирамидни и / или симптоми на отнемане, включително възбуда, хипертония, хипотония, тремор, сънливост, респираторен дистрес и съобщено е нарушение на храненето при новородени, чиито майки са били изложени на антипсихотични лекарства през третия триместър на бременността. Тези симптоми са варирали по тежест. Някои новородени се възстановяват в рамките на часове или дни без специфично лечение; други изискват продължителна хоспитализация. Следете новородените за екстрапирамидни и / или симптоми на отнемане и управлявайте симптомите по подходящ начин.
Данни
Данни за животни
В проучване за развитие на ембрио-плода бременните плъхове получават 4, 16 или 64 mg / kg / ден (1.6, 6.5 и 26 пъти повече от максимална препоръчителна доза при хора (MRHD) от 24 mg / ден на база mg / m2) илоперидон перорално през периода на органогенезата. Най-високата доза предизвиква увеличена ранна вътрематочна смърт, намалено тегло и дължина на плода, намалена скелетна скелетна плода и повишена честота на незначителни фетални аномалии на скелета и вариации; тази доза също предизвика намалена консумация на храна за майката и наддаване на тегло.
В изследване за развитие на ембрио-плода, бременни зайци са получавали 4, 10 или 25 mg / kg / ден (3, 8 и 20 пъти MRHD на mg / m2 основа) на илоперидон в периода на органогенезата. Най-високата доза предизвиква увеличена ранна вътрематочна смърт и намалена жизнеспособност на плода при термин; тази доза също причини токсичност за майката.
В допълнителни проучвания, при които на плъхове се дава илоперидон в дози, сходни с горните, започвайки или от предварителна концепция, или от ден 17 от бременността и продължавайки чрез отбиване, неблагоприятните репродуктивни ефекти включват продължителна бременност и раждане, увеличени процент на мъртвородени деца, увеличена честота на феталните висцерални изменения, намалено тегло на плода и малките и намалено тегло след раждане оцеляване. Нямаше лекарствени ефекти върху невробихевиоралното или репродуктивното развитие на оцелелите кученца. Дозите без ефект варират от 4 до 12 mg / kg с изключение на увеличаването на скоростта на мъртворождение, което се наблюдава при най-ниската тествана доза от 4 mg / kg, което е 1,6 пъти по-голямо от MRHD на mg / m2. При тези проучвания се наблюдава токсичност за майката при по-високите дози.
Метаболитът илоперидон P95, който е основен циркулиращ метаболит на илоперидон при хора, но не присъства в значителни количества при плъхове са били давани на бременни плъхове по време на органогенезата при перорални дози от 20, 80 или 200 mg кг / ден. Не са наблюдавани тератогенни ефекти. Закъсняла скелетна осификация се наблюдава при всички дози. Не се произвежда значителна токсичност за майката. Плазмените нива на P95 (AUC) при най-високата тествана доза са 2 пъти по-високи от тези при хора, получаващи MRHD на илоперидон.
Кърмене
Обобщение на риска
Няма информация относно наличието на илоперидон или неговите метаболити в кърмата ефекти на илоперидон върху кърмено дете, нито ефектите на илоперидон върху кърмата производство. Илоперидонът присъства в млякото от плъхове. Поради потенциала за сериозни нежелани реакции при кърмачета, посъветвайте жена да не кърми по време на лечение с FANAPT.
Данни Прехвърлянето на радиоактивност в млякото на кърмещи плъхове е изследвано след еднократна доза [14С] илоперидон при 5 mg / kg. Концентрацията на радиоактивност в мляко в 4 часа след дозата е била близо 10 пъти по-голяма от тази в плазмата едновременно. Въпреки това, до 24 часа след дозирането концентрациите на радиоактивност в млякото са паднали до стойности, малко по-ниски от плазмените. Метаболитният профил в млякото беше качествено подобен на този в плазмата.
Педиатрична употреба Безопасността и ефективността при педиатрични и юношески пациенти не са установени.
Гериатрична употреба
Клиничните изследвания на FANAPT при лечението на шизофрения не включват достатъчен брой от пациенти на възраст над 65 години, за да определят дали реагират по различен начин от по-младия пациенти. От 3210 пациенти, лекувани с FANAPT в проучвания преди пускане на пазара, 25 (0,5%) са на възраст ≥65 години и няма пациенти на възраст ≥ 75 години.
Пациенти в напреднала възраст с психоза, свързани с деменция, лекувани с FANAPT, са с повишен риск от смърт в сравнение с плацебо. FANAPT не е одобрен за лечение на пациенти с психоза, свързана с деменция.
Бъбречна недостатъчност
Тъй като FANAPT е силно метаболизиран, като по-малко от 1% от лекарството се екскретира непроменено, само бъбречното увреждане е малко вероятно да окаже значително влияние върху фармакокинетиката на FANAPT. Бъбречно увреждане (креатининов клирънс <30 mL / min) имаше минимален ефект върху Cmax на илоперидон (даден в еднократна доза от 3 mg) и неговите метаболити P88 и P95 във всеки от измерените 3аналити. AUC0– ∞ се увеличава с 24%, намалява с 6% и се увеличава съответно с 52% за илоперидон, P88 и P95 при лица с бъбречно увреждане.
Чернодробно увреждане
Не е необходимо адаптиране на дозата към FANAPT при пациенти с леко чернодробно увреждане. Пациенти с умерено чернодробно увреждане може да изискват намаляване на дозата. FANAPT не се препоръчва на пациенти с тежко чернодробно увреждане.
При възрастни лица с леко чернодробно увреждане не се наблюдава съответна разлика във фармакокинетиката на илоперидон, P88 или P95 (общо или несвързано) в сравнение със здрави контроли при възрастни. При лица с умерено чернодробно увреждане по-висока (2-кратна) и по-променлива свободна експозиция на активните метаболити P88 наблюдавани в сравнение със здрави контроли, докато експозицията на илоперидон и Р95 като цяло е сходна (по-малко от 50% промяна в сравнение с контрола). Тъй като не е провеждано проучване при пациенти с тежко увреждане на черния дроб, FANAPT не се препоръчва за пациенти с тежко чернодробно увреждане.
Състояние на пушенето
Въз основа на in vitro изследвания, използващи човешки чернодробни ензими, FANAPT не е субстрат за CYP1A2; следователно тютюнопушенето не трябва да има ефект върху фармакокинетиката на FANAPT.
бременност
Горна част
Злоупотреба с наркотици и зависимост
Контролирано вещество
FANAPT не е контролирано вещество.
злоупотреба
FANAPT не е изследван систематично при животни или хора поради потенциала му за злоупотреба, толерантност или физическа зависимост. Въпреки че клиничните изпитвания не разкриват тенденция за поведение на наркотици, тези наблюдения не са системни и не са възможни да прогнозира въз основа на този опит степента, в която едно активно лекарство на ЦНС, FANAPT, ще бъде злоупотребено, отклонено и / или злоупотребено веднъж пуснат на пазара. Следователно пациентите трябва да бъдат оценявани внимателно за анамнеза за злоупотреба с наркотици и такива трябва да бъдат наблюдава се отблизо за признаци на злоупотреба или злоупотреба с FANAPT (например развитие на толерантност, увеличаване на дозата, търсене на лекарство поведение).
Горна част
Предозирането
Човешки опит
В предварителните маркетингови проучвания, включващи над 3210 пациенти, е имало случайно или умишлено предозиране на FANAPT документирани при 8 пациенти, вариращи от 48 mg до 576 mg, приети наведнъж, и 292 mg приети за 3 дни месечен цикъл. Няма съобщения за смъртни случаи от тези случаи. Най-големият потвърден еднократен прием на FANAPT е 576 mg; не са отбелязани неблагоприятни физически ефекти при този пациент. Следващият най-голям потвърден прием на FANAPT е 438 mg за период от 4 дни; са докладвани екстрапирамидни симптоми и QTc интервал от 507 msec за този пациент без сърдечни последствия. Този пациент възобновява лечението с FANAPT за допълнителни 11 месеца.
Като цяло, съобщените признаци и симптоми са тези, които са резултат от преувеличаване на известните фармакологични ефекти (напр. Сънливост и седация, тахикардия и хипотония) на FANAPT.
Управление на предозиране
Няма специфичен антидот за FANAPT. Следователно трябва да се въведат подходящи подкрепящи мерки. В случай на остро предозиране, лекарят трябва да установи и поддържа дихателните пътища и да осигури адекватна оксигенация и вентилация. Трябва да се обмисли стомашна промивка (след интубация, ако пациентът е в безсъзнание) и прилагане на активен въглен заедно с слабително. Възможността за запушване, гърчове или дистонична реакция на главата и шията след предозиране може да създаде риск от аспирация с индуцирана повръщане. Сърдечно-съдовият мониторинг трябва да започне незабавно и трябва да включва непрекъснато наблюдение на ЕКГ за откриване на възможни аритмии. Ако се прилага антиаритмична терапия, дизопирамид, прокаинамид и хинидин не трябва да се използват, тъй като те имат потенциал за QT-удължаващи ефекти, които могат да бъдат адитивни към тези на FANAPT. По същия начин е разумно да се очаква, че алфа-блокиращите свойства на бретилия могат да бъдат добавъчни към тези на FANAPT, което води до проблемна хипотония. Хипотонията и кръвообращението трябва да се лекуват с подходящи мерки като интравенозни течности или симпатомиметични средства (не трябва да се използват епинефрин и допамин, тъй като бета стимулацията може да влоши хипотонията при настройка на алфа-индуцираната алфа блокада). В случаи на тежки екстрапирамидни симптоми трябва да се прилагат антихолинергични лекарства. Близкият медицински контрол трябва да продължи, докато пациентът не се възстанови.
Горна част
описание
FANAPT е нетипичен антипсихотик, принадлежащ към химичния клас на производни на пиперидинил-бензизоксазол. Химичното му наименование е 4 '- [3- [4- (6-флуоро-1,2-бензизоксазол-3-ил) пиперидино] пропокси] -3'-метоксиацетофенон. Молекулната му формула е C24H27FN2O4, а молекулното му тегло е 426.48. Структурната формула е:
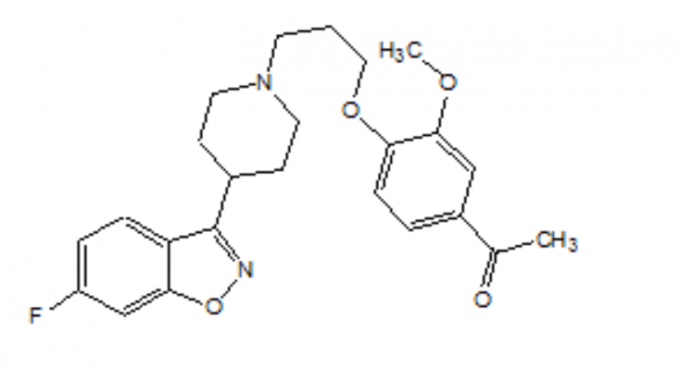
Илоперидонът е бял до почти бял фино кристален прах. Той е практически неразтворим във вода, много слабо разтворим в 0,1 N НС1 и свободно разтворим в хлороформ, етанол, метанол и ацетонитрил.
FANAPT таблетки са предназначени само за перорално приложение. Всеки кръг, без покритие
таблетка съдържа 1 mg, 2 mg, 4 mg, 6 mg, 8 mg, 10 mg или 12 mg илоперидон. Неактивните съставки са: лактоза монохидрат, микрокристална целулоза, хидроксипропилметилцелулоза, кросповидон, магнезиев стеарат, колоиден силиций
диоксид и пречистена вода (отстранява се по време на обработката). Таблетките са бели, кръгли, плоски, със скосени ръбове и се идентифицират с лого „”, вдлъбнато от едната страна и сила на таблета „1”, „2”, „4”, „6”, „8”, „10”, или „12”, релефно от другата страна.
Горна част
Клинична фармакология
Механизъм на действие
Механизмът на действие на илоперидон при шизофрения е неизвестен. Въпреки това ефикасността на илоперидон може да бъде медиирана чрез комбинация от антагонизъм на допамин тип 2 (D2) и серотонин тип 2 (5-НТ2).
Илоперидонът образува активен метаболит, P88, който има профил на свързване in vitro рецептор, подобен на основното лекарство.
Фармакодинамика
Илоперидонът действа като антагонист с високо (нМ) афинитетно свързване към серотонин 5-НТ2А допамин D2 и D3рецептори и норепинефрин NEα1 рецептори (Ki стойности от 5.6, 6.3, 7.1 и 0.36 пМ, съответно). Илоперидонът има умерен афинитет към допамин D4 и рецепторите за серотонин 5-HT6 и 5 -HT7 (Ki стойности на 25, 43 и 22, nM съответно) и нисък афинитет към рецепторите на серотонин 5-HT1A, допамин D1 и хистамин Н1 рецептори (Ki стойности на 168, 216 и 437 пМ, съответно). Илоперидонът няма значителен афинитет (Ki> 1000 пМ) към холинергичните мускаринови рецептори. Афинитетът на метаболит илоперидон P88 обикновено е равен или по-малък от този на изходното съединение, докато метаболитът P95 само показва афинитет към 5-HT2A (Ki стойност от 3,91) и рецепторите NEα1A, NEα1B, NEα1D и NEα2C (Ki стойности от 4,7, 2,7, 8,8 и 4,7 nM съответно).
Фармакокинетика
Наблюдаваният среден полуживот на илоперидон, P88 и P95 в обширни метаболизатори на CYP2D6 (EM) са съответно 18, 26 и 23 часа, а при лоши метаболизатори (ПМ) са съответно 33, 37 и 31 часа. Концентрациите в стационарно състояние се постигат в рамките на 3- 4 дни след приема. Натрупването на илоперидон се предвижда от фармакокинетиката на еднократна доза. Фармакокинетиката на илоперидон е повече от пропорционална на дозата. Елиминирането на илоперидон се осъществява главно чрез чернодробен метаболизъм, включващ 2 P450 изозими, CYP2D6 и CYP3A4.
Абсорбция: Iloperidone се абсорбира добре след прилагане на таблетката с пикови плазмени концентрации, настъпващи в рамките на 2 до 4 часа; докато относителната бионаличност на таблетния състав в сравнение с пероралния разтвор е 96%. Приложението на илоперидон със стандартна храна с високо съдържание на мазнини не повлиява значително Cmax или AUC на илоперидон, P88 или P95, но забавено Tmax с 1 час за илоперидон, 2 часа за P88 и 6 часа за P95. FANAPT може да се прилага независимо от храненето.
Разпределение: Iloperidone има видим клирънс (клирънс / бионаличност) от 47 до 102 L / h, с видим обем на разпределение 1340-2800 L. При терапевтични концентрации несвързаната фракция на илоперидон в плазмата е ~ 3%, а на всеки метаболит (P88 и P95) е ~ 8%.
Метаболизъм и елиминиране: Илоперидонът се метаболизира основно чрез 3 пътя на биотрансформация: редукция на карбонил, хидроксилиране (медиирано от CYP2D6) и О-деметилиране (медиирано от CYP3A4). Има 2 преобладаващи илоперидонови метаболити, P95 и P88. Метаболитът на илоперидон P95 представлява 47,9% от AUC на илоперидон и неговите метаболити в плазма в стационарно състояние за екстензивни метаболизатори (EM) и 25% за лоши метаболизатори (PM). Активният метаболит P88 представлява съответно 19,5% и 34,0% от общата плазмена експозиция в ЕМ и ПМ.
Приблизително 7% -10% от кавказците и 3% -8% чернокожи / афро-американците нямат капацитет да метаболизират CYP2D6 субстрати и се класифицират като лоши метаболизатори (ПМ), докато останалите са междинни, обширни или ултрабързи метаболизатори. Съвместното приложение на FANAPT с известни силни инхибитори на CYP2D6 като флуоксетин води до 2.3 пъти увеличаване на плазмената експозиция на илоперидон и следователно трябва да бъде половината от дозата FANAPT приложен.
По същия начин, ПМ на CYP2D6 имат по-висока експозиция на илоперидон в сравнение с ЕМ, а ПМ трябва да намалят дозата си с половина. Налични са лабораторни тестове за идентифициране на CYP2D6 PM.
По-голямата част от радиоактивните материали се възстановяват в урината (средно 58,2% и 45,1% съответно в ЕМ и ПМ), като изпражненията представляват 19,9% (ЕМ) до 22,1% (ПМ) от дозираната радиоактивност.
Транспортерно взаимодействие: Илоперидон и P88 не са субстрати на P-gp, а илоперидонът е слаб P-gp инхибитор.
Горна част
Неклинична токсикология
Канцерогенеза, мутагенеза, увреждане на плодовитостта
Канцерогенеза: Проучванията за канцерогенност през целия живот са проведени при мишки CD-1 и плъхове Sprague Dawley. Илоперидон се прилага перорално в дози от 2,5, 5,0 и 10 mg / kg / ден на мишки CD-1 и 4, 8 и 16 mg / kg / ден на Плъхове Sprague Dawley (0,5, 1,0 и 2,0 пъти и 1,6, 3,2 и 6,5 пъти, съответно, MRHD от 24 mg / ден на mg / m2 база). Имаше повишена честота на злокачествени тумори на млечната жлеза при женски мишки, лекувани само с най-ниската доза (2,5 mg / kg / ден). Не са наблюдавани свързани с лечението увеличения на неоплазия при плъхове.
Канцерогенният потенциал на метаболита илоперидон P95, който е основен циркулиращ метаболит на илоперидон при хора, но не присъства в значителни количества в мишки или плъхове, беше оценено при проучване за канцерогенност за цял живот при плъхове Wistar при перорални дози от 25, 75 и 200 mg / kg / ден при мъже и 50, 150 и 250 (намалени от 400) mg / kg / ден през женските. Свързани с лекарството неопластични промени са настъпили при мъжете, в хипофизната жлеза (pars distalis adenoma) при всички дози и в панкреаса (островния клетъчен аденом) при високата доза. Плазмените нива на P95 (AUC) при мъже в тестваните дози (25, 75 и 200 mg / kg / ден) са приблизително 0,4, 3 и 23 пъти, съответно, човешката експозиция на P95 при MRHD на илоперидон.
Мутагенеза: Илоперидонът е отрицателен при теста на Еймс и при in vivo тестовете за костен мозък на мишки и черния дроб на плъх. Хломозомни аберации, индуцирани от илоперидон, in vitro в клетки на яйчниците на Китайския хамстер (СНО) в концентрации, които също предизвикват известна цитотоксичност.
Метаболитът на илоперидон P95 е отрицателен при теста на Еймс, теста за аберация на хромозома V79 и in vivo тест за микронуклеус на костен мозък на мишка.
Нарушаване на фертилитета: Илоперидон намалява фертилитета при 12 и 36 mg / kg при проучване, в което са лекувани и мъжки, и женски плъхове. Дозата без ефект е 4 mg / kg, което е 1,6 пъти MRHD от 24 mg / ден на база mg / m2.
Горна част
Клинични изследвания
Ефикасността на FANAPT при лечението на шизофрения беше подкрепена от 2 плацебо и активно контролирани краткосрочни (4- и 6-седмични) изпитвания и едно дългосрочно плацебо-контролирано рандомизирано съдебен процес. Всички проучвания включват пациенти, които отговарят на критериите DSM-III / IV за шизофрения.
В тези проучвания бяха използвани три инструмента за оценка на психиатричните признаци и симптоми. Положителната и отрицателната скала на синдрома (PANSS) и кратката психиатрична скала за оценка (BPRS) са двата описания на много артикули.
от обща психопатология, обикновено използвана за оценка на ефектите от лекарственото лечение при шизофрения. Оценката на клиничната глобална импресия (CGI) отразява впечатлението на квалифициран наблюдател, напълно запознат с проявите на шизофрения, за цялостното клинично състояние на пациента.
6-седмично, плацебо-контролирано проучване (n = 706) включва 2 гъвкави диапазона на дозата FANAPT (12-16 mg / ден или 20-24 mg / ден) в сравнение с плацебо и активен контрол (рисперидон). За групата от 12-16 mg / ден схемата за титруване на FANAPT е 1 mg два пъти дневно на 1 и 2 дни, 2 mg два пъти дневно на 3 и 4 дни, 4 mg два пъти дневно на 5 и 6 дни и 6 mg два пъти всеки ден на 7-ми ден. За групата от 20-24 mg / ден схемата за титруване на FANAPT е 1 mg два пъти дневно на 1-ви ден, 2 mg два пъти дневно на 2-ри ден, 4 mg два пъти дневно на ден 3, 6 mg два пъти дневно на 4 и 5 дни, 8 mg два пъти дневно на 6 ден, и 10 mg два пъти дневно на 7 ден. Основната крайна точка беше промяна от изходната стойност на общия резултат на BPRS в края на лечението (Ден 42). Както диапазоните от 12-16 mg / ден и дозите от 20-24 mg / ден на FANAPT бяха по-добри от плацебо при общия резултат на BPRS. Изглежда, че активното контролно антипсихотично лекарство превъзхожда FANAPT в това изпитване в рамките на първите 2 седмици, констатация, която отчасти може да се обясни с по-бързото титруване, което беше възможно за това лекарство. При пациенти в това проучване, които остават на лечение най-малко 2 седмици, изглежда, че илоперидонът има сравнима ефективност с активната контрола.
4-седмично, плацебо-контролирано проучване (n = 604) включва една фиксирана доза FANAPT (24 mg / ден) в сравнение с плацебо и активна контрола (зипрасидон). Графикът на титруване на това проучване беше подобен на този за 6-седмичното проучване. Това проучване включва титруване на FANAPT, започващо с 1 mg два пъти дневно на 1-ви ден и увеличаване до 2, 4, 6, 8, 10 и 12 mg два пъти дневно на 2, 3, 4, 5, 6 и 7 ден. Основната крайна точка беше промяна от изходната стойност на общия резултат на PANSS в края на лечението (ден 28). Дозата FANAPT от 24 mg / ден е по-висока от плацебо в общия резултат на PANSS. Изглежда, че FANAPT има подобна ефикасност на активното контролно лекарство, което също се нуждае от бавно титруване до целевата доза.
В по-дългосрочно изпитване клинично стабилни амбулатории за възрастни (n = 303), отговарящи на критериите DSM-IV за шизофрения, които остават стабилни след 12 седмици от лечението с отворен етикет с гъвкави дози FANAPT (8 mg / ден - 24 mg / ден, прилагани като дози два пъти дневно) бяха рандомизирани на плацебо или да продължат на тяхната настояща доза FANAPT (8 mg / ден - 24 mg / ден, приложени като дози два пъти дневно) за наблюдение за възможен рецидив по време на двойно-сляп рецидив фаза на превенция. Стабилизацията по време на фазата с отворен етикет се определя като установена доза FANAPT, която е непроменена поради ефикасността в 4-те седмици преди рандомизацията, с оценка на CGI-сериозност ≤4 и обща оценка на PANSS ≤70, оценка ≤4 на всеки от следните отделни елементи на PANSS (P1-заблуди, P2-концептуална дезорганизация, P3-халюцинаторно поведение, P6 подозрителност / преследване, P7-враждебност или G8-некооперативност), и няма хоспитализация или повишаване на нивото на грижи за лечение обостряния. Рецидив или предстоящ рецидив по време на фазата на предотвратяване на двойно сляпо рецидиви се определя като всеки от следва: хоспитализация поради влошаване на шизофрения, увеличаване (влошаване) на общия резултат на PANSS ≥30%, CGI-
Резултат от подобрение ≥6, пациентът е имал самоубийствено, убийствено или агресивно поведение или нужда от друго антипсихотично лекарство.

Въз основа на междинния анализ независима комисия за наблюдение на данни реши, че проучването трябва да бъде прекратено рано поради доказателства за ефикасност. Въз основа на резултатите от междинния анализ, които бяха потвърдени от данните от крайния анализ, пациентите, лекувани с FANAPT има статистически значимо по-дълго време за рецидив или предстоящ рецидив, отколкото пациентите, които са получили плацебо. Фигура 1 показва приблизителната кумулативна част от пациентите с рецидив или предстоящ рецидив въз основа на крайния набор от данни.
Горна част
Как се доставят / съхранение и работа
Таблетките FANAPT са бели, кръгли и се идентифицират с лого, вдлъбнато от едната страна и със сила на таблета „1”, „2”, „4”, „6”, „8”, „10” или „12”, от другата. страна. Таблетките се доставят в следните силни страни и конфигурация на опаковката:

съхранение
Съхранявайте FANAPT таблетки при контролирана стайна температура, 25 ° C (77 ° F); екскурзии, разрешени до 15 ° до 30 ° C (59 ° до 86 ° F) [Вижте USP контролирана температура в помещението]. Защитете таблетките FANAPT от излагане на светлина и влага.
ИНФОРМАЦИЯ ЗА СЪХРАНЕНИЕ НА ПАЦИЕНТА
Лекарите се съветват да обсъждат следните проблеми с пациенти, за които предписват FANAPT:
QT интервал удължаване
Пациентите трябва да бъдат посъветвани да се консултират незабавно с лекаря си, ако се чувстват отпаднали, губят съзнание или сърцебиене. Пациентите трябва да бъдат съветвани да не приемат FANAPT с други лекарства, които причиняват удължаване на QT интервала. Пациентите трябва да бъдат информирани да информират лекарите, че приемат FANAPT, преди да бъдат приети нови лекарства.
Невролептичен злокачествен синдром
Пациентите и лицата, които се грижат за тях, трябва да бъдат съветвани, че понякога се препраща потенциално фатален симптомен комплекс както е съобщено за NMS във връзка с прилагането на антипсихотични лекарства, включително FANAPT. Признаците и симптомите на НМС включват хиперпирексия, мускулна ригидност, променен психичен статус и доказателства за автономност
нестабилност (неравномерен пулс или кръвно налягане, тахикардия, диафореза и сърдечна диритмия).
Метаболитни промени
Пациентите трябва да са наясно със симптомите на хипергликемия (висока кръвна захар) и захарен диабет. Пациенти с диагноза диабет, такива с рискови фактори за диабет или такива, които ги развиват симптомите по време на лечението трябва да бъдат следени кръвната им глюкоза в началото и периодично по време на лечение. Пациентите трябва да бъдат съветвани, че е настъпило повишаване на теглото по време на лечение с FANAPT. Препоръчва се клинично наблюдение на теглото.
Ортостатична хипотония
Пациентите трябва да бъдат информирани за риска от ортостатична хипотония, особено в момента на започване на лечението, повторно започване на лечение или увеличаване на дозата.
Намеса в когнитивните и двигателните характеристики
Тъй като FANAPT може да има потенциал да влоши преценката, мисленето или двигателните умения, пациентите трябва да бъдат предупредени експлоатация на опасни машини, включително автомобили, докато не бъдем сигурни, че терапията с FANAPT не ги засяга неблагоприятно.
бременност
Консултирайте пациентите, че употребата на Fanapt в третия триместър може да причини екстрапирамидни и / или симптоми на абстиненция при новородено. Консултирайте пациентите да уведомяват своя доставчик на здравно обслужване с известна или предполагаема бременност.
Регистър на бременността
Консултирайте пациентите, че има регистър на експозицията на бременност, който следи резултатите от бременността при жени, изложени на FANAPT по време на бременност
Кърмене
Консултирайте жените да не кърмят по време на лечение с FANAPT.
Съпътстващо лечение
Пациентите трябва да бъдат съветвани да информират лекарите си, ако приемат или планират да приемат лекарства, отпускани по лекарско предписание или без рецепта, тъй като има потенциал за взаимодействие.
алкохол
Пациентите трябва да бъдат съветвани да избягват алкохол, докато приемат FANAPT.
Излагане на топлина и дехидратация
Пациентите трябва да бъдат съветвани относно подходящите грижи за избягване на прегряване и дехидратация.
Разпространено от:
Vanda Pharmaceuticals Inc.
Вашингтон, D.C. 20037 САЩ
Vanda и Fanapt® са регистрирани търговски марки на Vanda Pharmaceuticals Inc. в САЩ и други страни.
Върнете се в началото
Ръководство за предписване на Fanapt (Iloperidone) (PDF)
Информацията в тази монография не е предназначена да обхване всички възможни употреби, указания, предпазни мерки, лекарствени взаимодействия или нежелани ефекти. Тази информация е обобщена и не е предназначена за конкретни медицински съвети. Ако имате въпроси относно лекарствата, които приемате или искате повече информация, консултирайте се с Вашия лекар, фармацевт или медицинска сестра.
последна актуализация 07/13
обратно към: Психиатрични лекарства Начална страница по фармакология


