Provigil: Лечение на будността (пълна предписваща информация)
Марка: Provigil
Родово име: Модафинил
Съдържание:
описание
фармакология
Клинични пътеки
Показания и употреба
Противопоказания
Предупреждения
предпазни мерки
Нежелани реакции
Злоупотреба с наркотици и зависимост
Предозирането
Дозировка и приложение
Как се доставя
Провигил (модафинил) информационен лист за пациента (на обикновен английски)
описание
Провигил (модафинил) е средство, стимулиращо събуждането при орално приложение. Модафинил е рацемично съединение. Химичното наименование на модафинил е 2 - [(дифенилметил) сулфинил] ацетамид. Молекулната формула е C15H15NO2S, а молекулното тегло е 273,35.
Химическата структура е:
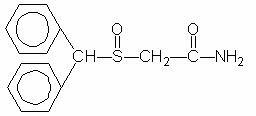
Модафинил е бял до почти бял кристален прах, който е практически неразтворим във вода и циклохексан. Той е умерено до слабо разтворим в метанол и ацетон. Провигил таблетки съдържат 100 mg или 200 mg модафинил и следните неактивни съставки: лактоза, микрокристална целулоза, предварително желатинизирано нишесте, кроскармелоза натрий, повидон и магнезий стеарат.
Горна част
Клинична фармакология
Механизъм на действие и фармакология
Точният механизъм (и), чрез които модафинил насърчава будността, не е известен. Модафинил има стимулиращи събуждането действия, подобни на симпатомиметични средства като амфетамин и метилфенидат, въпреки че фармакологичният профил не е идентичен с този на симпатомиметичните амини.
Модафинил има слабо до незначително взаимодействие с рецептори за норепинефрин, серотонин, допамин, GABA, аденозин, хистамин-3, мелатонин и бензодиазепини. Модафинил също не инхибира активността на МАО-В или фосфодиестерази II-V.
Индуцираното от модафинил будност може да бъде ограничено от β ± 1-адренергичния рецепторен антагонист празозин; Въпреки това, модафинил е неактивен в други ин витро системи за анализ, за които е известно, че реагират на Î ± -адренергични агонисти, като например препарата за вас семена за плъх.
Модафинил не е агонист на допаминовия рецептор с пряко или индиректно действие. Въпреки това, ин витро, модафинил се свързва с преносителя на допамин и инхибира обратното поемане на допамин. Тази активност се свързва in vivo с повишени нива на извънклетъчен допамин в някои мозъчни региони на животни. При генно-инженерни мишки, лишени от допаминов транспортер (DAT), на модафинил липсва активност, стимулираща събуждането, което предполага, че тази активност е зависима от DAT. Въпреки това, ефектите, стимулиращи събуждането, на модафинил, за разлика от тези на амфетамин, не са антагонизирани от антагониста на халоперидол на допаминовия рецептор при плъхове. В допълнение алфа-метил-р-тирозинът, инхибитор на синтеза на допамин, блокира действието на амфетамин, но не блокира локомоторната активност, индуцирана от модафинил.
При котката равни дози, стимулиращи будността, метилфенидат и амфетамин повишават активирането на невроните в целия мозък. Модафинил при еквивалентна доза, стимулираща будността, селективно и значително засилва активирането на невроните в по-дискретни области на мозъка. Връзката на тази находка при котки с ефектите на модафинил при хората е неизвестна.
В допълнение към своите стимулиращи ефекти при събуждане и способността да повишава опорно-двигателната активност при животни, модафинил произвежда психоактивни и еуфорични ефекти, промени в настроението, възприятието, мисленето и чувствата, характерни за други стимуланти на ЦНС при хората. Модафинил има подсилващи свойства, както се вижда от самоприлагането му при маймуни, преди това обучени за самостоятелно приложение на кокаин. Модафинил също беше частично дискриминиран като стимулант.
Оптичните енантиомери на модафинил имат подобно фармакологично действие при животни. Два основни метаболита на модафинил, модафинилова киселина и модафинил сулфон, изглежда, не допринасят за активиращите ЦНС свойства на модафинил.
Фармакокинетика
Модафинил е рацемично съединение, чиито енантиомери имат различна фармакокинетика (напр. Полуживотът на l-изомера е приблизително три пъти по-дълъг от d-изомера при възрастни хора). Енантиомерите не се преобразуват. В стационарно състояние общата експозиция на l-изомера е приблизително три пъти по-висока от тази на d-изомера. Нивото на концентрацията (С)minss) на циркулиращия модафинил след еднократна дневна доза се състои от 90% l-изомер и 10% от d-изомера. Ефективният елиминационен полуживот на модафинил след множество дози е около 15 часа. Енантиомерите на модафинил проявяват линейна кинетика при многократно дозиране от 200-600 mg / ден веднъж дневно при здрави доброволци. Очевидните стационарни състояния на общия модафинил и l - (-) - модафинил се постигат след 2-4 дни на дозиране.
абсорбция
Абсорбцията на таблетки Provigil е бърза, като пиковите плазмени концентрации се появяват на 2-4 часа. Бионаличността на таблетки Provigil е приблизително равна на тази на водна суспензия. Абсолютната орална бионаличност не се определя поради неразтворимостта на водата (<1 mg / mL) модафинил, което изключва интравенозно приложение. Храната няма ефект върху общата бионаличност на Provigil; обаче нейното усвояване (tмакс) може да се забави с приблизително един час, ако се приема с храна.
разпределение
Модафинил е добре разпределен в тъканите на тялото с видим обем на разпределение (~ 0,9 L / kg) по-голям от обема на общата вода в тялото (0,6 L / kg). В човешката плазма in vitro модафинилът се свързва умерено с плазмените протеини (~ 60%, главно с албумина). При серумни концентрации, получени в стабилно състояние след дози от 200 mg / ден, модафинил не показва изместване на протеиновото свързване на варфарин, диазепам или пропранолол. Дори при много по-големи концентрации (1000 uM; > 25 пъти Смакс от 40 uM в стационарно състояние при 400 mg / ден), модафинил няма ефект върху свързването на варфарин. Модафинилова киселина при концентрации> 500 uM намалява степента на свързване на варфарин, но тези концентрации са> 35 пъти по-високи от постигнатите терапевтично.
Метаболизъм и елиминиране
Основният начин на елиминиране е метаболизмът (~ 90%), главно от черния дроб, с последващо бъбречно елиминиране на метаболитите. Алкализирането на урината няма ефект върху елиминирането на модафинил.
Метаболизмът се осъществява чрез хидролитично дезамидиране, S-окисление, ароматна хидроксилация на пръстена и конюгиране с глюкуронид. По-малко от 10% от приложената доза се екскретира като основното съединение. В клинично проучване, използващо радиомаркиран модафинил, общо 81% от прилаганата радиоактивност се възстановява за 11 дни след приема, предимно в урината (80% спрямо 1,0% в изпражненията). Най-голямата част от лекарството в урината е модафинилова киселина, но поне шест други метаболити присъстват в по-ниски концентрации. Само два метаболита достигат до значими концентрации в плазмата, т.е. модафинилова киселина и модафинил сулфон. В предклинични модели модафинилова киселина, модафинил сулфон, 2 - [(дифенилметил) сулфонил] оцетна киселина и 4-хидрокси модафинил не са били активни или не изглежда да медиират възбудителните ефекти на модафинил.
При възрастни понякога се наблюдават понижения на нивата на модафинил след многоседмично дозиране, което предполага автоиндукция, но големината на пониженията и несъответствието на тяхната поява подсказват, че тяхната клинична значимост е минимален. Наблюдава се значително натрупване на модафинил сулфон след многократни дози поради дългия му елиминационен полуживот от 40 часа. Индукция на метаболизиращи ензими, най-вече цитохром Р-450 (CYP) 3A4, също е наблюдавана in vitro след инкубация на първични култури на човешки хепатоцити с модафинил и in vivo след продължително приложение на модафинил при 400 mg / ден. (За по-нататъшно обсъждане на ефектите на модафинил върху ензимните дейности на CYP вижте МЕРКИ, Лекарствени взаимодействия.)
Взаимодействия с лекарства:
Въз основа на in vitro данните модафинил се метаболизира частично от 3А изоформеното подсемейство на чернодробния цитохром Р450 (CYP3A4). В допълнение, модафинил има потенциала да инхибира CYP2C19, потиска CYP2C9 и индуцира CYP3A4, CYP2B6 и CYP1A2. Тъй като модафинил и модафинил сулфон са обратими инхибитори на лекарствения метаболизиращ ензим CYP2C19, съвместното приложение на модафинил с лекарства като диазепам, фенитоин и пропранолол, които до голяма степен се елиминират по този път, могат да повишат нивата на циркулация на тези съединения. В допълнение, при хора с дефицит на ензима CYP2D6 (т.е. 7-10% от населението на Кавказ; подобни или по-ниски при други популации) нивата на субстрати на CYP2D6 като трициклични антидепресанти и селективен серотонин инхибиторите на обратното захващане, които имат спомагателни пътища на елиминиране чрез CYP2C19, могат да бъдат увеличени чрез едновременно приложение на модафинил. Може да са необходими корекции на дозата за пациенти, лекувани с тези и подобни лекарства (виж МЕРКИ, Лекарствени взаимодействия). Изследване in vitro показа, че армодафинил (един от енантиомерите на модафинил) е субстрат на Р-гликопротеин.
Едновременното приложение на модафинил с други активни лекарства от ЦНС като метилфенидат и декстроамфетамин не променя значително фармакокинетиката на нито едно от двете лекарства.
Установено е, че хроничното приложение на 400 mg модафинил намалява системната експозиция на два CYP3A4 субстрати, етинил естрадиол и триазолам след перорално приложение предполага, че CYP3A4 е бил индуциран. Хроничното приложение на модафинил може да увеличи елиминирането на субстрати на CYP3A4. Може да са необходими корекции на дозата за пациенти, лекувани с тези и подобни лекарства (виж МЕРКИ, Лекарствени взаимодействия).
Наблюдава се очевидно свързано с концентрацията потискане на активността на CYP2C9 при човешки хепатоцити след излагане на модафинил in vitro предполагайки, че има потенциал за метаболитно взаимодействие между модафинил и субстратите на този ензим (например, S-варфарин, фенитоин). Въпреки това, в проучване за взаимодействие при здрави доброволци, хроничното лечение с модафинил не показва значителен ефект върху фармакокинетиката на варфарин в сравнение с плацебо. (Виж МЕРКИ, Лекарствени взаимодействия, други лекарства, варфарин).
Специални популации
Полов ефект:
Фармакокинетиката на модафинил не се влияе от пола.
Възраст ефект:
Леко намаление (~ 20%) на оралния клирънс (CL / F) на модафинил се наблюдава при еднократно проучване с доза от 200 mg в 12 субекти със средна възраст от 63 години (диапазон 53 - 72 години), но смята се, че промяната не е клинична значимо. В проучване за многократна доза (300 mg / ден) при 12 пациенти със средна възраст от 82 години (в границите 67 - 87 години), средната нивата на модафинил в плазмата са приблизително два пъти по-високи от исторически получените при съчетани по-млади субекти. Поради потенциални ефекти от множеството съпътстващи лекарства, с които повечето пациенти са били третирани, очевидната разлика във фармакокинетиката на модафинил може да не се дължи само на ефектите на стареене. Резултатите обаче предполагат, че клирънсът на модафинил може да бъде намален при възрастни хора (виж Дозировка и приложение).
Състезателен ефект:
Влиянието на расата върху фармакокинетиката на модафинил не е проучено.
Бъбречна недостатъчност:
При еднократна доза от 200 mg модафинил, тежка хронична бъбречна недостатъчност (креатининов клирънс ‰ mL 20 mL / min) не повлияват значително фармакокинетиката на модафинил, но експозицията на модафинилова киселина (неактивен метаболит) е увеличена 9-кратна (Вж МЕРКИ).
Чернодробно увреждане:
Фармакокинетиката и метаболизмът са изследвани при пациенти с цироза на черния дроб (6 мъже и 3 жени). Трима пациенти са имали цироза на стадий В или В + (по критериите на детето), а 6 пациенти са имали стадий С или С + цироза. Клинично 8 от 9 пациенти са били иктерични и всички имат асцит. При тези пациенти оралният клирънс на модафинил е намален с около 60% и концентрацията в стационарно състояние е удвоена в сравнение с нормалните пациенти. Дозата на Provigil трябва да бъде намалена при пациенти с тежко чернодробно увреждане (Вж МЕРКИ и Дозировка и приложение).
Горна част
Клинични пътеки
Ефективността на Provigil за намаляване на прекомерната сънливост е установена при следващия сън нарушения: нарколепсия, обструктивна сънна апнея / синдром на хипопнея (OSAHS) и разстройство на работния сън (SWSD).
Нарколепсия
Ефективността на Provigil за намаляване на прекомерната сънливост (ES), свързана с нарколепсия, е установена през две американски 9-седмични, мултицентрови, плацебо контролирани, две дози (200 mg на ден и 400 mg на ден), паралелни групи, двойно слепи изследвания на амбулаторни пациенти, които са се запознали с Критерии ICD-9 и Американската асоциация на съня разстройства за нарколепсия (които също са в съответствие с Американската психиатрична асоциация DSM-IV критерии). Тези критерии включват или 1) повтарящи се дневни сънливи или пропадания в съня, които се появяват почти ежедневно в продължение на най-малко три месеца, плюс внезапна двустранна загуба на постурален мускулен тонус във връзка с интензивна емоция (катаплексия) или 2) оплакване от прекомерна сънливост или внезапна мускулна слабост със свързани характеристики: парализа на съня, хипнагогични халюцинации, автоматично поведение, нарушен основен сън епизод; и полисомнография, демонстрираща едно от следните: латентност на съня по-малко от 10 минути или бързо движение на очите (REM) латентност на съня по-малко от 20 минути. Освен това, за да влязат в тези проучвания, от всички пациенти се изисква обективно документирано прекомерно сънливост през деня, многократен сън Тест за латентност (MSLT) с два или повече REM периода на сън и отсъствие на други клинично значими активни медицински или психиатрични разстройство. MSLT, обективна дневна полисомнографска оценка на способността на пациента да заспи при нестимулиращ околна среда, измерва закъснение (в минути) за начало на съня средно за 4 тестови сесии на интервали от 2 часа след нощни часове полисомнография. За всяка тестова сесия на субекта е казано да лежи тихо и да се опитва да заспи. Всяка сесия за тестване беше прекратена след 20 минути, ако не се случи сън или 15 минути след началото на съня.
И в двете проучвания основните мерки за ефективност са 1) латентност на съня, оценена от теста за поддържане на будност (MWT) и 2) промяната в цялостния статус на пациента, измерена от Клиничното глобално впечатление за промяна (CGI-C). За успешното изпитване и двете мерки трябваше да покажат значително подобрение.
MWT измерва латентността (в минути) за началото на съня средно за 4 тестови сесии на интервали от 2 часа след нощна полисомнография. За всяка тестова сесия субектът беше помолен да се опита да остане буден, без да използва извънредни мерки. Всяка сесия за тестване беше прекратена след 20 минути, ако не се случи сън или 10 минути след началото на съня. CGI-C е 7-точкова скала, съсредоточена без промяна и варираща от много много по-лошо до много подобрено. Пациентите са оценени от оценители, които нямат достъп до каквито и да било данни за пациентите, освен до мярка за тяхната основна тежест. Оценителите не получиха конкретни указания относно критериите, които трябва да се прилагат при оценяване на пациенти.
Други оценки на ефекта включват Тест за множествена латентност на съня (MSLT), Скала за сънливост на Epworth (ESS; поредица от въпроси, предназначени да оценят степента на сънливост в ежедневните ситуации) Тестът за явна производителност на Steer (SCPT; компютърно базирана оценка на способността на пациента да избягва удрянето на препятствия в симулирана ситуация на шофиране), стандартна нощна полисомнография и дневен дневник на съня на пациента. Пациентите също бяха оценявани с скалата Качество на живот в нарколепсия (QOLIN), която съдържа валидирания здравен въпросник SF-36.
И двете проучвания показват подобрение на обективни и субективни мерки за прекомерна дневна сънливост както за дозите от 200 mg, така и за 400 mg в сравнение с плацебо. Пациентите, лекувани с която и да е доза от Provigil, показват статистически значително повишена способност да остават будни на MWT (всички р стойности <0,001) при 3, 6, 9 седмици и последно посещение в сравнение с плацебо и статистически значително по-голямо глобално подобрение, както е оценено по скалата CGI-C (всички p стойности <0.05).
Средната продължителност на съня (в минути) на MWT в началната линия за 2 контролирани изпитвания е показана в таблица 1 по-долу, заедно със средната промяна от базовата линия на MWT при окончателно посещение.
Процентите на пациентите, които показват каквато и да е степен на подобрение на CGI-C в двете клинични изпитвания, са показани в таблица 2 по-долу.
Подобни статистически значими подобрения, свързани с лечението, се наблюдават и при други мерки за обезценка през 2008 г нарколепсия, включително пациент, оценен нивото на сънливост през деня на ESS (р <0,001 за всяка доза в сравнение с плацебо).
Нощният сън, измерен с полисомнография, не се повлиява от употребата на Provigil.
Обструктивна сънна апнея / Синдром на хипопнея (OSAHS)
Ефективността на Provigil за намаляване на прекомерната сънливост, свързана с OSAHS, е установена в две клинични проучвания. И в двете проучвания са включени пациенти, които отговарят на Международната класификация на нарушенията на съня (ICSD) критерии за OSAHS (които също са в съответствие с Американската психиатрична асоциация DSM-IV критерии). Тези критерии включват или: 1) прекомерна сънливост или безсъние, плюс чести епизоди на увреждане дишане по време на сън и свързани функции като силен хъркане, сутрешно главоболие и сухота в устата при пробуждане; или 2) прекомерна сънливост или безсъние и полисомнография, демонстриращи едно от следните: повече от пет обструктивни апнеи, всяка с продължителност над 10 секунди, на час на съня и едно или повече от изброените по-долу: чести възбуди от съня, свързани с апнеите, брадитахикардия и десатурация на артериален кислород във връзка с нарушаване на дишането. В допълнение, за влизане в тези проучвания се изискваше всички пациенти да имат прекомерна сънливост, както беше показано с резултат 10 on на скалата за сънливост на Epworth, въпреки лечението с постоянно положително налягане на дихателните пътища (СРАР). Необходимо е доказателство, че CPAP е ефективен за намаляване на епизодите на апнея / хипопнея, заедно с документация за използването на CPAP.
В първото проучване, 12-седмично многоцентрово плацебо-контролирано проучване, общо 327 пациенти бяха рандомизирани да получават Provigil 200 mg / ден, Provigil 400 mg / ден или съответстващо плацебо. По-голямата част от пациентите (80%) са напълно съобразени с CPAP, дефиниран като CPAP употреба> 4 часа / нощ на> 70% нощувки. Останалите частично са съвместими с CPAP, дефинирани като CPAP ползване на 30% нощувки. Използването на CPAP продължи през цялото проучване. Основните мерки за ефективност са: 1) латентност на съня, оценена от теста за поддържане на будност (MWT) и 2) промяна в цялостния статус на пациента, измерена от Клиничното глобално впечатление за промяна (CGI-C) на 12-та седмица или последната посетите. (Виж Клинични пътеки, Раздел за нарколепсия по-горе за описание на тези тестове.)
Пациентите, лекувани с Provigil, показват статистически значимо подобрение на способността за остават будни в сравнение с лекуваните с плацебо пациенти, измерени с MWT (р <0,001) в крайна точка [Маса 1]. Пациентите, лекувани с провигил, също показват статистически значимо подобрение на клиничното състояние, оценено по скалата CGI-C (p <0,001) [Таблица 2]. Двете дози Provigil изпълниха по подобен начин.
Във второто проучване, 4-седмично многоцентрово плацебо-контролирано проучване, 157 пациенти са били рандомизирани или с Provigil 400 mg / ден, или с плацебо. За всички пациенти е необходима документация за редовна употреба на CPAP (най-малко 4 часа / нощ при 70% от нощите). Основната мярка за резултат беше промяната от основната линия на ESS на 4-та седмица или окончателно посещение. Основните ESS резултати за групите Provigil и плацебо са съответно 14,2 и 14,4. На 4-та седмица ESS е намален с 4,6 в групата на Provigil и с 2,0 в групата на плацебо, разлика, която е статистически значима (p <0,0001).
Нощният сън, измерен с полисомнография, не се повлиява от употребата на Provigil.
Разстройство на работния сън при смяна (SWSD)
Ефективността на Provigil за прекомерната сънливост, свързана със SWSD, е доказана в 12-седмично плацебо-контролирано клинично проучване. Общо 209 пациенти с хроничен SWSD бяха рандомизирани да получават Provigil 200 mg / ден или плацебо. Всички пациенти отговаряха на критериите за хронична SWSD (които са) на Международната класификация на нарушенията на съня (ICSD-10) в съответствие с критериите на DSM-IV на Американската психиатрична асоциация за нарушение на съня в циркадния ритъм: работа на смени Тип). Тези критерии включват 1) или: а) първично оплакване от прекомерна сънливост или безсъние, което е свързано временно с период на работа (обикновено нощна работа), възниква по време на фазата на обичайния сън или б) полисомнографията и MSLT демонстрират загуба на нормален модел сън-събуждане (т.е. нарушен хронобиологичен ритмичност); и 2) никакви други медицински или психически разстройства не отчитат симптомите и 3) симптомите не отговарят на критериите за всяко друго разстройство на съня, което води до безсъние или прекомерна сънливост (например промяна на часовата зона [джет лаг] синдром).
Трябва да се отбележи, че не всички пациенти с оплакване от сънливост, които също са ангажирани с работа на смени, отговарят на критериите за диагнозата на SWSD. В клиничното изпитване са били включени само пациенти, които са били симптоматични поне 3 месеца.
Записаните пациенти също трябваше да работят минимум 5 нощни смени на месец, да имат прекомерна сънливост в време на нощните им смени (MSLT резултат <6 минути) и дневно безсъние се документира с дневна полисомнограма (PSG).
Основните мерки за ефективност са 1) латентност на съня, оценена от теста за многократна латентност на съня (MSLT), извършен по време на симулирана нощна смяна на 12-та седмица или окончателното посещение и 2) промяната в общия статус на пациента, измерена от Клиничното глобално впечатление за промяна (CGI-C) на 12-та седмица или окончателното посетите. Пациентите, лекувани с Provigil, показват статистически значимо удължаване на времето за начало на съня в сравнение с лекуваните с плацебо пациенти, измерени с нощния MSLT [Таблица 1] (p <0,05). Наблюдава се също, че подобрението на CGI-C е статистически значимо (p <0,001). (Виж Клинични пътеки, Раздел за нарколепсия по-горе за описание на тези тестове.)
Дневният сън, измерен с полисомнография, не се повлиява от употребата на Provigil.
HTML клипборд
| смущение | Мярка | Провиджил 200 mg * |
Провиджил 400 mg * |
Плацебо | |||
| * Значително различен от плацебо за всички изпитвания (p <0,01 за всички изпитвания, но SWSD, което е p <0,05) | |||||||
| Изходна | промяна от Базова линия |
Изходна | промяна от Базова линия |
Изходна | Промяна от Изходна |
||
| Нарколепсия I | MWT | 5.8 | 2.3 | 6.6 | 2.3 | 5.8 | -0.7 |
| Нарколепсия II | MWT | 6.1 | 2.2 | 5.9 | 2.0 | 6.0 | -0.7 |
| OSAHS | MWT | 13.1 | 1.6 | 13.6 | 1.5 | 13.8 | -1.1 |
| SWSD | MSLT | 2.1 | 1.7 | - | - | 2.0 | 0.3 |
| смущение | Провиджил 200 mg * |
Провиджил 400 mg * |
Плацебо |
| * Значително различен от плацебо за всички изпитвания (p <0.01) | |||
| Нарколепсия I | 64% | 72% | 37% |
| Нарколепсия II | 58% | 60% | 38% |
| OSAHS | 61% | 68% | 37% |
| SWSD | 74% | - | 36% |
Горна част
Показания и употреба
Provigil е показан за подобряване на будността при възрастни пациенти с прекомерна сънливост, свързана с нарколепсия, обструктивна сънна апнея / синдром на хипопнея и нарушение на работния сън при смяна.
В OSAHS Provigil е показан като допълнение към стандартното (ите) лечение (и) за основната обструкция. Ако непрекъснатото положително налягане на дихателните пътища (CPAP) е лечение на избор за пациент, трябва да се положат максимални усилия за лечение с CPAP за адекватен период от време, преди започване на лечение с Provigil. Ако Provigil се използва допълнително с CPAP, е необходимо насърчаване и периодична оценка на съответствието на CPAP.
Във всички случаи внимателното внимание към диагнозата и лечението на основното нарушение на съня е от изключително значение. Предписващите лекари трябва да знаят, че някои пациенти могат да имат повече от едно нарушение на съня, което допринася за прекомерната им сънливост.
Ефективността на модафинил при продължителна употреба (по-голяма от 9 седмици при клинични изпитвания за нарколепсия и 12 седмици в клиничните изпитвания за OSAHS и SWSD) не е систематично оценяван при плацебо контролирани изпитвания. Лекарят, който реши да предпише Provigil за продължителен период от време при пациенти с нарколепсия, OSAHS или SWSD, трябва периодично да преоценява дългосрочната полезност за отделния пациент.
Горна част
Противопоказания
Провигил е противопоказан при пациенти с известна свръхчувствителност към модафинил, армодафинил или неговите неактивни съставки.
Горна част
Предупреждения
Сериозен обрив, включително синдромът на Стивънс-Джонсън
Съобщава се за сериозен обрив, изискващ хоспитализация и прекратяване на лечението при възрастни и деца във връзка с употребата на модафинил.
Модафинил не е одобрен за употреба при педиатрични пациенти за никакви показания.
В клинични изпитвания на модафинил честотата на обрив, водещ до прекратяване, е приблизително 0.8% (13 на 1585) при педиатрични пациенти (възраст <17 години); тези обриви включваха 1 случай на възможен синдром на Стивънс-Джонсън (SJS) и 1 случай на очевидна реакция на свръхчувствителност на много органи. Няколко от случаите са били свързани с треска и други отклонения (напр. Повръщане, левкопения). Средното време до обрив, което доведе до прекратяване, беше 13 дни. Не са наблюдавани такива случаи сред 380 педиатрични пациенти, които са получавали плацебо. Не са съобщени сериозни кожни обриви при клинични изпитвания при възрастни (0 на 4,264) модафинил.
Редки случаи на сериозен или животозастрашаващ обрив, включително SJS, токсична епидермална некролиза (TEN) и лекарствена обрива с Има съобщения за еозинофилия и системни симптоми (DRESS) при възрастни и деца в целия постмаркетингов маркетинг по света опит. Коефициентът на отчитане на TEN и SJS, свързан с употребата на модафинил, който обикновено се приема за подценяване поради недостатъчно отчитане, надвишава честотата на фона на честотата. Прогнозите за степента на честота на фона на тези сериозни кожни реакции в общата популация варират между 1 до 2 случая на милион души години.
Не са известни фактори, които да прогнозират риска от поява или тежестта на обрива, свързан с модафинил. Почти всички случаи на сериозен обрив, свързан с модафинил, се появяват в рамките на 1 до 5 седмици след започване на лечението. Има съобщения за изолирани случаи след продължително лечение (например, 3 месеца). Съответно, продължителността на терапията не може да се разчита като средство за прогнозиране на потенциалния риск, предявен от първата поява на обрив.
Въпреки че доброкачествените обриви се срещат и с модафинил, не е възможно надеждно да се предвиди кои обриви ще се окажат сериозни. Съответно модафинил обикновено трябва да се прекрати при първите признаци на обрив, освен ако очевидно обривът не е свързан с лекарството. Прекратяването на лечението може да не попречи на обрива да стане животозастрашаващ или трайно да се деактивира или обезобрази.
Ангиоедем и анафилактоидни реакции
Един сериозен случай на ангиоедем и един случай на свръхчувствителност (с обрив, дисфагия и бронхоспазъм) са били наблюдаван сред 1595 пациенти, лекувани с армодафинил, R енантиомер на модафинил (който е рацемичният смес). Не са наблюдавани такива случаи при клинични проучвания на модафинил. Съобщава се обаче за ангиоедем при постмаркетингов опит с модафинил. Пациентите трябва да бъдат посъветвани да преустановят терапията и незабавно да докладват на своя лекар за някакви признаци или симптоми, предполагащи ангиоедем или анафилаксия (например подуване на лицето, очите, устните, езика или ларинкса; затруднено преглъщане или дишане; пресипналост).
Реакции на свръхчувствителност на много органи
Има реакции на свръхчувствителност на много органи, включително поне една фатална смърт в постмаркетинговия опит възникна в тясна временна асоциация (средно време до откриване 13 дни: диапазон 4-33) до началото на модафинил.
Въпреки че има ограничен брой съобщения, реакциите на свръхчувствителност на много органи могат да доведат до хоспитализация или да бъдат животозастрашаващи. Не са известни фактори, които да прогнозират риска от поява или тежестта на реакциите на мултиорганна свръхчувствителност, свързани с модафинил. Признаците и симптомите на това разстройство бяха разнообразни; въпреки това, пациентите обикновено, макар и не изключително, са с треска и обрив, свързани с участието на други органи. Други свързани прояви включват миокардит, хепатит, нарушения в теста на чернодробната функция, хематологични отклонения (напр. еозинофилия, левкопения, тромбоцитопения), сърбеж и астения. Тъй като многоорганна свръхчувствителност е променлива в своята експресия, могат да се появят други симптоми и признаци на органна система, които не са отбелязани тук.
Ако се подозира реакция на свръхчувствителност на много органи, Провигил трябва да се прекрати. Въпреки че няма съобщения за случаи, които да показват кръстосана чувствителност към други лекарства, които произвеждат този синдром, опитът с лекарства, свързани с многоорганна свръхчувствителност, показва, че това е а възможност.
Постоянна сънливост
Пациентите с анормални нива на сънливост, които приемат Provigil, трябва да бъдат информирани, че нивото им на будност може да не се върне към нормалното. Пациентите с прекомерна сънливост, включително тези, които приемат Provigil, трябва да бъдат често преоценявани за тяхната степен на сънливост и, ако е подходящо, се препоръчва да се избягва шофиране или друга потенциално опасна дейност. Предписващите лекари също трябва да са наясно, че пациентите може да не признават сънливост или сънливост, докато не бъдат директно поставени под въпрос за сънливост или сънливост по време на специфични дейности.
Психични симптоми
Има съобщения за психиатрични нежелани проучвания при пациенти, лекувани с модафинил. След непрофесионалните събития след пускането на пазара, свързани с употребата на модафинил, са включени мания, заблуди, халюцинации, самоубийствена идея и агресия, някои от които водят до хоспитализация. Много, но не всички пациенти са имали предишна психиатрична анамнеза. Един здрав мъжки доброволец разработи идеи за референция, параноични заблуди и слухови халюцинации във връзка с множество дневни дози модафинил от 600 mg и лишаване от сън. Няма данни за психоза 36 часа след прекратяване на лекарството.
В базата данни за проучвания с контролирани модафинил при възрастни психиатрични симптоми, водещи до прекратяване на лечението (с честота> 0,3%) и докладвани по-често при пациенти лекувани с модафинил в сравнение с лекуваните с плацебо са били тревожност (1%), нервност (1%), безсъние (<1%), объркване (<1%), възбуда (<1%) и депресия (<1%), Трябва да се подхожда с повишено внимание, когато Provigil се прилага на пациенти с анамнеза за психоза, депресия или мания. Трябва да се обмисли възможната поява или изостряне на психиатричните симптоми при пациенти, лекувани с Provigil. Ако психиатричните симптоми се развият във връзка с приложението на Provigil, помислете за прекратяване на приложението на Provigil.
Горна част
предпазни мерки
Диагностика на нарушения на съня
Provigil трябва да се използва само при пациенти, които са преценили пълната си сънливост и при които а диагнозата на нарколепсия, OSAHS и / или SWSD е поставена в съответствие с критериите за диагностика на ICSD или DSM (виж Клинични пътеки). Такава оценка обикновено се състои от пълна история и физикален преглед и може да бъде допълнена с тестване в лабораторни условия. Някои пациенти могат да имат повече от едно нарушение на съня, което допринася за прекомерната им сънливост (например, OSAHS и SWSD съвпадат при един и същ пациент).
Общ
Въпреки че не е доказано, че модафинил предизвиква функционално увреждане, всяко лекарство, засягащо ЦНС, може да промени преценката, мисленето или двигателните умения. Пациентите трябва да бъдат предупредени да работят с автомобил или други опасни машини, докато не са разумно е сигурно, че терапията с Provigil няма да повлияе неблагоприятно върху способността им да участват в такова дейности.
Използване на CPAP при пациенти с OSAHS
В OSAHS Provigil е показан като допълнение към стандартното (ите) лечение (и) за основната обструкция. Ако непрекъснатото положително налягане на дихателните пътища (CPAP) е лечение на избор за пациент, трябва да се положат максимални усилия за лечение с CPAP за адекватен период от време, преди започване на лечение с Provigil. Ако Provigil се използва допълнително с CPAP, е необходимо насърчаване и периодична оценка на съответствието на CPAP.
Сърдечносъдова система
Модафинил не е оценяван при пациенти с скорошна анамнеза за инфаркт на миокарда или нестабилна стенокардия и такива пациенти трябва да се лекуват с повишено внимание.
В клинични проучвания на Provigil, признаци и симптоми, включително болка в гърдите, сърцебиене, диспнея и преходна исхемия Промени в Т-вълната на ЕКГ са наблюдавани при три лица във връзка с пролапс на митралната клапа или лявата камера хипертрофия. Препоръчва се таблетките Provigil да не се прилагат при пациенти с анамнеза за хипертрофия на лявата камера или пациенти с пролапс на митралната клапа, които са изпитали синдрома на пролапса на митралната клапа, когато преди това са получавали ЦНС стимуланти. Такива признаци могат да включват, но не се ограничават до исхемични промени в ЕКГ, болка в гърдите или аритмия. Ако се появи ново проявление на някой от тези симптоми, помислете за сърдечна оценка.
Проследяването на кръвното налягане в краткосрочни (<3 месеца) контролирани проучвания не показва клинично значимо промени в средното систолно и диастолично кръвно налягане при пациенти, получаващи Provigil в сравнение с плацебо. Въпреки това, ретроспективен анализ на употребата на антихипертензивни лекарства в тези проучвания показа, че по-голяма част от пациентите на Provigil изискват нова или увеличена употреба на антихипертензивни лекарства (2,4%) в сравнение с пациенти на плацебо (0,7%). Диференциалното използване е малко по-голямо, когато се включват само проучвания при OSAHS, при 3,4% от пациентите Провигил и 1,1% от пациентите на плацебо, изискващи такива промени при употребата на антихипертензивни средства медикаменти. Повишеното наблюдение на кръвното налягане може да бъде подходящо при пациенти на Provigil.
Пациенти, използващи стероидни контрацептиви
Ефективността на стероидните контрацептиви може да бъде намалена, когато се използва с таблетки Provigil и един месец след прекратяване на терапията (вж. предпазни мерки, Лекарствени взаимодействия). Алтернативни или съпътстващи методи за контрацепция се препоръчват за пациенти, лекувани с таблетки Provigil, и един месец след прекратяване на приложението на Provigil.
Пациенти, използващи циклоспорин
Нивата на циклоспорин в кръвта могат да бъдат намалени, когато се използва с Провигил (Виж предпазни мерки, Лекарствени взаимодействия). Трябва да се обмисли мониторинг на циркулиращите концентрации на циклоспорин и подходящо коригиране на дозата за циклоспорин, когато тези лекарства се използват едновременно.
Пациенти с тежко чернодробно увреждане
При пациенти с тежко чернодробно увреждане, със или без цироза (Виж Клинична фармакология), Provigil трябва да се прилага в намалена доза (Вж Дозировка и приложение).
Пациенти с тежко бъбречно увреждане
Няма достатъчно информация за определяне на безопасността и ефикасността на дозирането при пациенти с тежко бъбречно увреждане. (За фармакокинетиката при бъбречно увреждане вж Клинична фармакология.)
Пациенти в напреднала възраст
При пациенти в напреднала възраст елиминирането на модафинил и неговите метаболити може да бъде намалено в резултат на стареене. Следователно трябва да се обмисли използването на по-ниски дози при тази популация. (Виж Клинична фармакология и Дозировка и приложение).
Информация за пациенти
Лекарите се съветват да обсъждат следните проблеми с пациенти, за които предписват Provigil.
Provigil е показан за пациенти, които имат анормални нива на сънливост. Доказано е, че Provigil подобрява, но не елиминира тази ненормална склонност към заспиване. Следователно пациентите не трябва да променят своето предишно поведение по отношение на потенциално опасни дейности (например шофиране, работа с машини) или други дейности, изискващи подходящи нива на будност, докато и освен ако не е показано, че лечението с Provigil води до нива на будност, които позволяват такова дейности. Пациентите трябва да бъдат информирани, че Provigil не е заместител на съня.
Пациентите трябва да бъдат информирани, че може да бъде критично, че те продължават да предприемат предписаните по-рано лечения (напр. Пациенти с OSAHS, получаващи CPAP, трябва да продължат да го правят).
Пациентите трябва да бъдат информирани за наличието на листовка с информация за пациента и трябва да бъдат инструктирани да прочетат листовката преди да приемат Provigil.
Пациентите трябва да бъдат посъветвани да се свържат с лекаря си, ако изпитват болка в гърдите, обрив, депресия, тревожност или признаци на психоза или мания.
бременност
Пациентите трябва да бъдат съветвани да уведомяват своя лекар, ако забременеят или възнамеряват да забременеят по време на терапията. Пациентите трябва да бъдат предупредени относно потенциалния повишен риск от бременност, когато използват стероидни контрацептиви (включително депо или имплантируеми противозачатъчни) с Provigil и в продължение на един месец след прекратяване на терапията (Вижте Карциногенеза, Мутагенеза, Увреждане на фертилитета и Бременност).
кърмене
Пациентите трябва да бъдат съветвани да уведомяват своя лекар, ако кърмят бебе.
Съпътстващо лечение
Пациентите трябва да бъдат съветвани да информират своя лекар, ако приемат или планират да приемат лекарства с рецепта или без рецепта, поради потенциала за взаимодействие между Provigil и други лекарства.
алкохол
Пациентите трябва да бъдат информирани, че употребата на Provigil в комбинация с алкохол не е проучена. Пациентите трябва да бъдат съветвани, че е разумно да избягват алкохола, докато приемат Провигил.
Алергични реакции
Пациентите трябва да бъдат посъветвани да спрат да приемат Provigil и да уведомят своя лекар, ако развият обрив, копривна треска, язви в устата, мехури, пилинг на кожата, проблеми с преглъщането или дишането или свързана с тях алергия феномен.
Взаимодействия с лекарства
CNS Активни лекарства
Метилфенидат
В проучване с еднократна доза при здрави доброволци, едновременно приложение на модафинил (200 mg) с метилфенидатът (40 mg) не предизвиква значителни промени във фармакокинетиката на нито една от двете лекарство. Обаче абсорбцията на Provigil може да се забави с приблизително един час, когато се прилага едновременно с метилфенидат.
В многократно дозирано стационарно проучване при здрави доброволци модафинил се прилага веднъж дневно при 200 mg / ден в продължение на 7 дни, последван от 400 mg / ден в продължение на 21 дни. Прилагане на метилфенидат (20 mg / ден) през 22-28 дни лечение с модафинил 8 часа след това дневната доза модафинил не предизвиква значителни изменения във фармакокинетиката на модафинил.
декстроамфетамин
В едно проучване с еднократна доза при здрави доброволци, едновременно приложение на модафинил (200 mg) с декстроамфетамин (10 mg) не предизвиква значителни промени във фармакокинетиката на нито една от двете лекарство. Въпреки това, абсорбцията на Provigil може да се забави с приблизително един час, когато се прилага едновременно с декстроамфетамин.
В многократно дозирано стационарно проучване при здрави доброволци модафинил се прилага веднъж дневно при 200 mg / ден в продължение на 7 дни, последван от 400 mg / ден в продължение на 21 дни. Приложение на декстроамфетамин (20 mg / ден) през 22-28 дни лечение с модафинил 7 часа след дневната доза модафинил не предизвиква значителни изменения във фармакокинетиката на модафинил.
Кломипраминът
Едновременното приложение на еднократна доза кломипрамин (50 mg) през първия от три дни лечение с модафинил (200 mg / ден) при здрави доброволци не показва ефект върху фармакокинетиката на нито едно от лекарствата. Съобщава се обаче за един инцидент с повишени нива на кломипрамин и неговия активен метаболит дезметилкломипрамин при пациент с нарколепсия по време на лечение с модафинил.
триазолам
В проучването на лекарственото взаимодействие между Provigil и etinyl estradiol (EE2), в същите дни като тези за при вземането на проби от плазмата за фармакокинетиката на EE2, се прилага и еднократна доза триазолам (0,125 mg). Средният Cmax и AUC0-β на триазолам са намалени съответно с 42% и 59% и полуживотът му на елиминиране е намален с приблизително час след лечението с модафинил.
Инхибитори на моноаминооксидазата (МАО)
Не са провеждани проучвания за взаимодействие с инхибитори на моноаминооксидазата. Следователно, трябва да се внимава при едновременно приложение на МАО инхибитори и модафинил.
Други лекарства
Варфарин
Не са наблюдавани значими промени във фармакокинетичните профили на R- и S-варфарин при здрави индивиди, получаващи еднократна доза рацемичен варфарин (5 mg) след хронично приложение на модафинил (200 mg / ден в продължение на 7 дни, последвано от 400 mg / ден в продължение на 27 дни) спрямо профилите на пациентите плацебо. Въпреки това, по-честото наблюдение на протромбиновите пъти / INR е препоръчително, когато Provigil се прилага едновременно с варфарин (виж Клинична фармакология, Фармакокинетика, лекарствени взаимодействия).
Етинил естрадиол
Прилагане на модафинил на доброволци жени веднъж дневно по 200 mg / ден в продължение на 7 дни, последвано от 400 mg / ден в продължение на 21 дни доведе до средно 11% намаление на Cmax и 18% спад в AUC0-24 на етинил естрадиол (ЕЕ2; 0,035 mg; прилага се перорално с норгестимат). Няма видима промяна в степента на елиминиране на етинил естрадиол.
Циклоспорин
Съобщава се за един случай на взаимодействие между модафинил и циклоспорин, субстрат на CYP3A4, при жена на 41 години, претърпяла трансплантация на органи. След едномесечен прием на 200 mg модафинил на ден нивата на циклоспорина в кръвта са намалени с 50%. Взаимодействието се предполага, че се дължи на засиления метаболизъм на циклоспорина, тъй като никой друг фактор, който се очаква да повлияе на разположението на лекарството, не се е променил. Може да се наложи корекция на дозата за циклоспорин.
Потенциални взаимодействия с лекарства, които инхибират, индуцират или се метаболизират от цитохром Р-450 изоензими и други чернодробни ензими
При in vitro проучвания, използващи първични човешки хепатоцитни култури, е показано, че модафинил леко индуцира CYP1A2, CYP2B6 и CYP3A4 по начин, зависим от концентрацията. Въпреки че резултатите от индукцията, основани на in vitro експерименти, не са непременно предсказващи реакцията in vivo, повишено внимание трябва да се упражнява, когато Provigil се прилага едновременно с лекарства, които зависят от тези три ензима клирънс. По-конкретно, могат да доведат до по-ниски нива в кръвта на такива лекарства (Вижте Други лекарства, Циклоспорине над).
Излагането на човешки хепатоцити на модафинил in vitro доведе до очевидно свързано с концентрацията потискане на експресията на активността на CYP2C9 предполагайки, че има потенциал за метаболитно взаимодействие между модафинил и субстратите на този ензим (например, S-варфарин и фенитоин). В последващо клинично проучване при здрави доброволци, хроничното лечение с модафинил не показва значителен ефект върху фармакокинетиката на еднократна доза варфарин в сравнение с плацебо (вж. предпазни мерки, Лекарствени взаимодействия, Варфарин).
Проучвания in vitro, използващи човешки чернодробни микрозоми, показват, че модафинил обратимо инхибира CYP2C19 при фармакологично значими концентрации на модафинил. CYP2C19 също се инхибира обратимо, с подобна сила, от циркулиращ метаболит, модафинил сулфон. Въпреки че максималните плазмени концентрации на модафинил сулфон са много по-ниски от тези на родителските модафинил, комбинираният ефект на двете съединения може да доведе до продължително частично инхибиране на ензим. Лекарства, които до голяма степен се елиминират чрез метаболизма на CYP2C19, като диазепам, пропранолол, фенитоин (също чрез CYP2C9) или S-мефенитоинът може да има продължително елиминиране при едновременно приложение с Provigil и може да изисква намаляване на дозата и мониторинг за токсичност.
Трициклични антидепресанти
CYP2C19 също осигурява спомагателен път за метаболизма на някои трициклични антидепресанти (например, кломипрамин и дезипрамин), които се метаболизират главно от CYP2D6. При трициклично лекувани пациенти с дефицит на CYP2D6 (т.е. тези, които са бедни метаболизатори на дебризоквин; 7-10% от населението на Кавказ; подобни или по-ниски при други популации), количеството на метаболизма от CYP2C19 може значително да се увеличи. Провигил може да причини повишаване на нивата на трицикличните при тази подгрупа пациенти. Лекарите трябва да знаят, че при тези пациенти може да е необходимо намаляване на дозата трициклични средства.
В допълнение, поради частичното участие на CYP3A4 в метаболитното елиминиране на модафинил, съвместното приложение на мощни индуктори на CYP3A4 (напр. карбамазепин, фенобарбитал, рифампин) или инхибитори на CYP3A4 (например, кетоконазол, итраконазол) могат да променят плазмените нива на модафинил.
Канцерогенеза, мутагенеза, увреждане на плодовитостта
Канцерогенеза
Проведени са проучвания за канцерогенност, при които модафинил се прилага в диетата на мишки за 78 седмици и на плъхове за 104 седмици в дози от 6, 30 и 60 mg / kg / ден. Най-високата изследвана доза е 1,5 (мишка) или 3 (плъх) пъти по-голяма от препоръчителната дневна доза модафинил (200 mg) за възрастни хора на база mg / m2. Няма данни за туморогенеза, свързана с приложението на модафинил при тези проучвания. Въпреки това, тъй като изследването при мишки използва неадекватно висока доза, която не е представителна за максимално поносима доза, последващо изследване за канцерогенност е проведено в Tg. AC трансгенна мишка. Дози, оценени в Tg. АС анализът е 125, 250 и 500 mg / kg / ден, прилаган дермално. Няма данни за туморогенност, свързана с приложението на модафинил; този дермален модел обаче може да не оцени адекватно канцерогенния потенциал на перорално прилаганото лекарство.
мутагенеза
Модафинил не показва доказателства за мутагенен или кластогенен потенциал в серия от in vitro (т.е., бактериален обратен мутационен анализ, миши лимфом tk анализ, хромозомна аберация анализ на човешки лимфоцити, анализ на клетъчна трансформация в BALB / 3T3 миши ембрионални клетки) анализ при липса или присъствие на метаболитна активация, или in vivo (микронуклеус на костен мозък на мишката) анализи. Модафинил също е отрицателен при непланирания анализ на ДНК синтеза в хепатоцитите на плъхове.
Нарушаване на плодовитостта
Перорално приложение на модафинил (дози до 480 mg / kg / ден) на мъжки и женски плъхове преди и по време на чифтосването и продължаването на женските през 7-ия гестационен ден доведе до увеличаване на времето за чифтосване най-високо дозата; не са наблюдавани ефекти върху други фертилни или репродуктивни параметри. Дозата без ефект от 240 mg / kg / ден е свързана с плазмената експозиция на модафинил (AUC), приблизително равна на тази при хора при препоръчителната доза от 200 mg.
бременност
Категория на бременността:
В проучвания, проведени при плъхове и зайци, е наблюдавана токсичност за развитие при клинично значими експозиции.
Модафинил (50, 100 или 200 mg / kg / ден), прилаган орално на бременни плъхове през целия период на причинена органогенеза, при липса на токсичност за майката, увеличаване на резорбциите и повишена честота на висцерални и скелетни изменения в потомството при най-високите доза. По-високата доза без ефект при токсичност за развитие на ембриофетални плъхове е свързана с плазма експозиция на модафинил приблизително 0,5 пъти AUC при хора при препоръчителната дневна доза (RHD) от 200 mg. Въпреки това, в последващо изследване до 480 mg / kg / ден (плазмена експозиция на модафинил, приблизително 2 пъти по-висока от AUC при хора при RHD) не са наблюдавани неблагоприятни ефекти върху развитието на ембриофетала.
Модафинил, прилаган през устата на бременни зайци през целия период на органогенеза в дози 45, 90 и 180 mg / kg / ден увеличава честотата на структурните изменения на плода и ембриофеталната смърт при най-високата доза. Най-високата доза без ефект за токсичност за развитие е свързана с плазмен AUC на модафинил, приблизително равен на AUC при хора при RHD.
Перорално приложение на армодафинил (R-енантиомер на модафинил; 60, 200 или 600 mg / kg / ден) за бременни плъхове през целия период на органогенеза, довело до увеличаване на честотата на фетални висцерални и скелетни изменения при междинната доза или по-големи и намалени тегла на плода на най-високото доза. Дозата без ефект за ембриофетална токсичност за развитие на плъх е свързана с плазмен армодафинил експозиция (AUC) приблизително една десета от AUC за армодафинил при хора, лекувани с модафинил при RHD.
Приложението на модафинил на плъхове по време на бременност и кърмене при перорални дози до 200 mg / kg / ден води до намаляване жизнеспособност на потомството при дози, по-големи от 20 mg / kg / ден (плазмен AUC на модафинил приблизително 0,1 пъти AUC при хора при RHD). Не са наблюдавани ефекти върху постнаталното развитие и параметрите на невробихевиоралните при оцелелите потомства.
Няма адекватни и добре контролирани проучвания при бременни жени. Съобщават се два случая на вътрематочно забавяне на растежа и един случай на спонтанен аборт във връзка с армодафинил и модафинил. Въпреки че фармакологията на модафинил и армодафинил не е идентична с тази на симпатомиметичните амини, те споделят някои фармакологични свойства с този клас. Някои от тези лекарства са свързани с вътрематочно забавяне на растежа и спонтанни аборти. Дали докладваните случаи са свързани с наркотици, не се знае.
Модафинил трябва да се използва по време на бременност, само ако потенциалната полза оправдава потенциалния риск за плода.
Труд и доставка
Ефектът на модафинил върху раждането и раждането при хора не е изследван систематично.
Кърмещи майки
Не е известно дали модафинил или неговите метаболити се екскретират в кърмата. Тъй като много лекарства се екскретират в кърмата, трябва да се внимава, когато Provigil таблетки се прилагат на кърмачка.
Педиатрична употреба
Безопасността и ефективността при педиатрични пациенти под 16-годишна възраст не са установени. Сериозни кожни обриви, включително мултиформен еритема (EMM) и синдром на Stevens-Johnson (SJS), са свързани с употребата на модафинил при педиатрични пациенти (вж. Предупреждения, Сериозен обрив, включително синдром на Стивънс-Джонсън).
В контролирано 6-седмично проучване 165 педиатрични пациенти (на възраст 5-17 години) с нарколепсия са лекувани с модафинил (n = 123) или плацебо (n = 42). Няма статистически значими разлики, благоприятстващи модафинил спрямо плацебо при удължаване на латентността на съня като измерена с MSLT или във възприятията за сънливост, както се определя от клиничната скала за глобално впечатление-клиницист (CGI-C).
В контролираните и отворени клинични проучвания, лекуваните нежелани събития на психиатричната и нервната система включва синдром на Турет, безсъние, враждебност, увеличена катаплексия, повишени хипнагогични халюцинации и самоубийства мисли. Наблюдава се и преходна левкопения, която се разрешава без лекарска намеса. В контролираното клинично проучване 3 от 38 момичета, на възраст 12 или повече години, лекувани с модафинил, са имали дисменорея в сравнение с 0 от 10 момичета, които са получавали плацебо.
Гериатрична употреба
Безопасността и ефективността при лица над 65 години не са установени. Опитът при ограничен брой пациенти на възраст над 65 години в клинични проучвания показва честота на нежелани преживявания, подобни на други възрастови групи.
Горна част
Нежелани реакции
Модафинил е оценен за безопасност при над 3500 пациенти, от които повече от 2000 пациенти с наднормено тегло сънливост, свързана с първични нарушения на съня и будността, се дава най-малко една доза от модафинил. В клинични проучвания е установено, че модафинил като цяло се понася добре и повечето нежелани реакции са леки до умерени.
Най-често наблюдаваните нежелани събития (‰ ¥ 5%), свързани с употребата на Provigil по-често, отколкото пациенти, лекувани с плацебо при плацебо-контролирани клинични проучвания при първични нарушения на съня и будността са главоболие, гадене, нервност, ринит, диария, болки в гърба, безпокойство, безсъние, виене на свят и диспепсия. Профилът на нежеланите събития беше подобен при тези проучвания.
В плацебо-контролираните клинични проучвания 74 от 934 пациенти (8%), които са приемали Provigil, са прекратени поради неблагоприятен опит в сравнение с 3% от пациентите, получавали плацебо. Най-честите причини за прекратяване, възникнали с по-висока скорост на Provigil от плацебо пациентите са главоболие (2%), гадене, тревожност, замаяност, безсъние, болки в гърдите и нервност (всеки <1%). В канадско клинично изпитване 35-годишен затлъстял нарколептичен мъж с предишна анамнеза за синкопални епизоди преживели 9-секунден епизод на асистолия след 27 дни лечение с модафинил (300 mg / ден разделено дози).
Честота в контролирани изпитвания
Следващата таблица (Таблица 3) представя нежеланите преживявания, възникнали със скорост 1% или повече и са по-чести при възрастни пациенти, лекувани с Provigil, отколкото при пациенти, лекувани с плацебо в главната клиника, контролирана с плацебо изпитвания.
Лекуващият лекар трябва да е наясно, че представените по-долу фигури не могат да се използват за прогнозиране на честотата на вредните преживявания при курс на обичайната медицинска практика, при който характеристиките на пациента и други фактори могат да се различават от тези, които се проявяват по време на клиничните проучвания. По подобен начин цитираните честоти не могат да бъдат сравнени директно с цифри, получени от други клинични изследвания, включващи различни лечения, употреби или изследователи. Прегледът на тези честоти обаче дава на лекуващите лекари основа за оценка на относителния принос на лекарствените и нелекарствените фактори към честотата на нежеланите събития в изследваната популация.
| Система на тялото | Предпочитан срок | Модафиниловата (n = 934) |
Плацебо (n = 567) |
| * Шест двойно слепи, плацебо-контролирани клинични проучвания при нарколепсия, OSAHS и SWSD. 1 Включват се събития, докладвани от поне 1% от пациентите, лекувани с Provigil, които са по-чести, отколкото в групата на плацебо; честотата се закръгля до най-близкия 1%. Терминологията за неблагоприятен опит се кодира с помощта на стандартен модифициран речник COSTART. Събития, за които честотата на Provigil е била най-малко 1%, но равна или по-малка от плацебо, не са посочени в таблицата. Тези събития включват следното: инфекция, болка, случайно нараняване, коремна болка, хипотермия, алергична реакция, астения, треска, вирусна инфекция, болка във врата, мигрена и др. ненормална електрокардиограма, хипотония, разстройство на зъбите, повръщане, периодонтален абсцес, повишен апетит, екхимоза, хипергликемия, периферен оток, загуба на тегло, тегло печалба, миалгия, крампи на краката, артрит, катаплексия, нарушения в мисленето, нарушение на съня, засилена кашлица, синузит, диспнея, бронхит, обрив, конюнктивит, болки в ушите, дисменорея4, инфекция на пикочните пътища. 2 Повишени чернодробни ензими. 3 Орофациални дискинезии. 4 Честота, коригирана според пола. | |||
| Тяло като цяло | главоболие | 34% | 23% |
| Болка в гърба | 6% | 5% | |
| Синдром на грип | 4% | 3% | |
| Болка в гърдите | 3% | 1% | |
| втрисане | 1% | 0% | |
| Ригидност на шията | 1% | 0% | |
| сърдечносъдов | Хипертония | 3% | 1% |
| тахикардия | 2% | 1% | |
| сърцебиене | 2% | 1% | |
| Вазодилатаци | 2% | 0% | |
| храносмилателната система | гадене | 11% | 3% |
| диария | 6% | 5% | |
| Диспепсия | 5% | 4% | |
| Суха уста | 4% | 2% | |
| анорексия | 4% | 1% | |
| запек | 2% | 1% | |
| Ненормална функция на черния дроб2 | 2% | 1% | |
| метеоризъм | 1% | 0% | |
| Улцерация на устата | 1% | 0% | |
| жажда | 1% | 0% | |
| Hemic / лимфната | еозинофилия | 1% | 0% |
| Метаболитният / Хранителна | оток | 1% | 0% |
| нервен | нервност | 7% | 3% |
| Безсъние | 5% | 1% | |
| безпокойство | 5% | 1% | |
| виене на свят | 5% | 4% | |
| депресия | 2% | 1% | |
| Парестезия | 2% | 0% | |
| сънливост | 2% | 1% | |
| Хипертония | 1% | 0% | |
| дискинезия3 | 1% | 0% | |
| хиперкинезия | 1% | 0% | |
| възбуда | 1% | 0% | |
| объркване | 1% | 0% | |
| треперене | 1% | 0% | |
| Емоционална лабилност | 1% | 0% | |
| световъртеж | 1% | 0% | |
| дихателен | ринит | 7% | 6% |
| фарингит | 4% | 2% | |
| Белодробно разстройство | 2% | 1% | |
| епистаксис | 1% | 0% | |
| астма | 1% | 0% | |
| Кожа / придатъци | изпотяване | 1% | 0% |
| Херпес симплекс | 1% | 0% | |
| Специални сетива | амблиопия | 1% | 0% |
| Ненормално зрение | 1% | 0% | |
| Вкус извратеност | 1% | 0% | |
| Болка в очите | 1% | 0% | |
| урогениталния | Аномалия на урината | 1% | 0% |
| Хематурия | 1% | 0% | |
| пиуриа | 1% | 0% |
Зависимост от дозата на нежеланите събития
В клинични проучвания, контролирани с плацебо при възрастни, които сравняват дози от 200, 300 и 400 mg на ден Провигил и плацебо, единствените нежелани събития, които бяха ясно свързани с дозата, са главоболие и тревожност.
Промени в жизнения знак
Въпреки че не е имало постоянна промяна в средните стойности на сърдечната честота или систолното и диастоличното кръвно налягане, изискването за антихипертензивни лекарства е малко по-голямо при пациенти на Provigil в сравнение с плацебо (Виж предпазни мерки).
Промени в теглото
Няма клинично значими разлики в промяната на телесното тегло при пациенти, лекувани с Provigil в сравнение с лекувани с плацебо пациенти в плацебо-контролираните клинични проучвания.
Лабораторни промени
Параметрите на клиничната химия, хематологията и урината са наблюдавани във фаза 1, 2 и 3 проучвания. При тези проучвания е установено, че средните плазмени нива на гама глутамилтрансфераза (GGT) и алкална фосфатаза (AP) са по-високи след приложението на Provigil, но не и плацебо. Малко лица обаче са имали повишаване на GGT или AP извън нормалните граници. Преминаването към по-високи, но не клинично значимо анормални стойности на GGT и AP изглежда се увеличават с времето в популацията, лекувана с Provigil във фаза 3 клинични проучвания. Не са установени различия в аланин аминотрансфераза, аспартат аминотрансфераза, общ протеин, албумин или общ билирубин.
Промени в ЕКГ
В клиничните проучвания, контролирани от плацебо, след прилагане на Provigil не е установен модел на възникване на лечението на ЕКГ.
Отчети за постмаркетинг
Следните нежелани реакции са установени по време на употребата на Provigil след одобрение. Тъй като тези реакции се съобщават доброволно от популация с несигурен размер, не е възможно надеждно да се прецени тяхната честота или да се установи причинно-следствена връзка с експозицията на лекарства. Решенията за включване на тези реакции в етикетирането обикновено се основават на един или повече от следните фактори: (1) сериозност на реакцията, (2) честота на докладване или (3) сила на причинно-следствената връзка с Провиджил.
Хематологична: агранулоцитоза
Горна част
Злоупотреба с наркотици и зависимост
Клас на контролирани вещества
Модафинил (Provigil) е посочен в приложение IV на Закона за контролирани вещества.
Злоупотреба с потенциал и зависимост
В допълнение към своя стимулиращ ефект на будността и повишена опорно-двигателна активност при животни, при хората, Provigil произвежда психоактивни и еуфорични ефекти, промени в настроението, възприятието, мисленето и чувствата, характерни за други стимуланти на ЦНС. При in vitro проучвания за свързване, модафинил се свързва към мястото на обратно захващане на допамин и причинява увеличаване на извънклетъчния допамин, но не увеличава освобождаването на допамин. Модафинил е засилващ, както се доказва от самоприлагането му при маймуни, предварително обучени за самостоятелно приложение на кокаин. В някои проучвания модафинилът също е частично дискриминиран като стимулант. Лекарите трябва да следят внимателно пациентите, особено тези с анамнеза за злоупотреба с наркотици и / или стимуланти (напр. Метилфенидат, амфетамин или кокаин). Пациентите трябва да бъдат наблюдавани за признаци на злоупотреба или злоупотреба (например, увеличаване на дозите или поведение, търсещо лекарство).
Потенциалът за злоупотреба с модафинил (200, 400 и 800 mg) е оценен по отношение на метилфенидат (45 и 90 mg) при стационарно проучване при лица с опит за злоупотреба с наркотици. Резултатите от това клинично проучване показват, че модафинил предизвиква психоактивни и еуфорични ефекти и чувства, съответстващи на други планирани стимуланти на ЦНС (метилфенидат).
оттегляне
Ефектите от оттеглянето на модафинил се наблюдават след 9 седмици употреба на модафинил в едно клинично изпитание, контролирано от фаза 3 в САЩ. Не са наблюдавани специфични симптоми на отнемане по време на 14-дневно наблюдение, въпреки че сънливостта се връща при нарколептични пациенти.
Горна част
Предозирането
Човешки опит
В клинични проучвания общо 151 протоколно определени дози, вариращи от 1000 до 1600 mg / ден (5 до 8 пъти повече от препоръчителната дневна доза от 200 mg) са били прилагани на 32 лица, включително 13 лица, които са получавали дози от 1000 или 1200 mg / ден в продължение на 7 до 21 последователни дни. Освен това са настъпили няколко умишлени остри свръхдози; двата най-големи са 4500 mg и 4000 mg, взети от двама участници, участващи в чуждестранни проучвания за депресия. Нито един от тези пациенти не е имал неочаквани или животозастрашаващи ефекти. Нежеланите реакции, докладвани при тези дози, включват възбуждане или възбуда, безсъние и леко или умерено повишаване на хемодинамичните параметри. Други наблюдавани ефекти при високи дози в клиничните проучвания включват тревожност, раздразнителност, агресивност, объркване, нервност, тремор, сърцебиене, нарушения на съня, гадене, диария и намален протромбин време.
От опит след пускане на пазара не са съобщени за фатални предози, включващи само модафинил (дози до 12 грама). Предозирането, включващо множество лекарства, включително модафинил, е довело до фатални резултати. Симптомите, които най-често съпътстват предозиране с модафинил, самостоятелно или в комбинация с други лекарства, включват: безсъние; симптоми на централната нервна система като безпокойство, дезориентация, объркване, възбуждане и халюцинация; храносмилателни промени като гадене и диария; и сърдечно-съдови промени като тахикардия, брадикардия, хипертония и гръдна болка.
Съобщавани са случаи на случайно поглъщане / предозиране при деца на възраст само на 11 месеца. Най-високото съобщено случайно поглъщане на база mg / kg е наблюдавано при тригодишно момче, което е приемало 800-1000 mg (50-63 mg / kg) модафинил. Детето остана стабилно. Симптомите, свързани с предозиране при деца, са били подобни на тези, наблюдавани при възрастни.
Управление на предозиране
Досега не е установен специфичен антидот за токсичните ефекти на предозиране на модафинил. Такива свръхдози трябва да се управляват с основно поддържаща грижа, включително сърдечно-съдов мониторинг. Ако няма противопоказания, трябва да се обмисли индуцирана повръщане или промиване на стомаха. Няма данни, които да предполагат полезността на диализата или подкисляването на урината или алкализирането за подобряване на елиминирането на лекарствата. Лекарят трябва да обмисли контакт с център за контрол на отровата за лечение на всякакво предозиране.
Горна част
Дозировка и приложение
Препоръчителната доза Provigil е 200 mg, дадени веднъж дневно.
За пациенти с нарколепсия и OSAHS, Provigil трябва да се приема като единична доза сутрин.
За пациенти със SWSD, Provigil трябва да се приема приблизително 1 час преди началото на работната смяна.
Дозите до 400 mg / ден, дадени като единична доза, се понасят добре, но няма последователни доказателства, че тази доза предоставя допълнителна полза извън тази на дозата от 200 mg (вж. Клинична фармакология и Клинични пътеки).
Общи съображения
Трябва да се обмисли коригиране на дозата за съпътстващи лекарства, които са субстрати за CYP3A4, като триазолам и циклоспорин (вж. предпазни мерки, Лекарствени взаимодействия).
Лекарства, които до голяма степен се елиминират чрез метаболизма на CYP2C19, като диазепам, пропранолол, фенитоин (също чрез CYP2C9) или S-мефенитоинът може да има продължително елиминиране при едновременно приложение с Provigil и може да изисква намаляване на дозата и мониторинг за токсичност.
При пациенти с тежко чернодробно увреждане, дозата Провигил трябва да бъде намалена до половината от препоръчителната за пациенти с нормална чернодробна функция (Вижте CКлинична фармакология и предпазни мерки).
Няма достатъчно информация за определяне на безопасността и ефикасността на дозирането при пациенти с тежко бъбречно увреждане (Виж Клинична фармакология и предпазни мерки).
При пациенти в напреднала възраст елиминирането на Provigil и неговите метаболити може да бъде намалено в резултат на стареене. Затова трябва да се обмисли използването на по-ниски дози при тази популация (виж Клинична фармакология и предпазни мерки).
Горна част
Как се доставя
Провиджил® (модафинил) Таблетки
100 mg: Всяка бяла, без покритие таблетка във формата на капсула е деболирана с "Provigil" от едната страна и "100 MG" от другата.
NDC 63459-101-01 - Бутилки от 100
200 mg: Всяка таблетка с форма на капсула, бяла, набрашнена, без покритие, е деболирана с "Provigil" от едната страна и "200 MG" от другата.
NDC 63459-201-01 - Бутилки от 100
Да се съхранява при 20 ° - 25 ° C (68 ° - 77 ° F).
Произведено за:
Cephalon, Inc.
Frazer, PA 19355
Американски патентни номера. RE37,516 / 4,927,855
© Cephalon, Inc., 2008. Всички права запазени
PROV-011
Последна актуализация: 03/08
Провигил (модафинил) информационен лист за пациента (на обикновен английски)
Подробна информация за Признаци, симптоми, причини, лечение на нарушения на съня
Информацията в тази монография не е предназначена да обхване всички възможни употреби, указания, предпазни мерки, лекарствени взаимодействия или нежелани ефекти. Тази информация е обобщена и не е предназначена за конкретни медицински съвети. Ако имате въпроси относно лекарствата, които приемате или искате повече информация, консултирайте се с Вашия лекар, фармацевт или медицинска сестра.
обратно към:
~ всички статии за нарушения на съня

